Перейти к:
Клинико-рентгенологическая диагностика гипофизита: обзор литературы и собственные наблюдения
https://doi.org/10.14341/probl12777
Аннотация
В настоящей статье представлен обзор литературы, посвященный особенностям клинического течения различных форм гипофизита, а также проблемам лучевой диагностики и лечения данной патологии. Гипофизит является малоизученным и многофакторным заболеванием, сложность диагностики которого обусловлена не только разнообразными неспецифическими клиническими проявлениями, данными гормонального исследования, но и неоднозначными результатами МРТ-исследования, отсутствием четких МР-паттернов. Данный обзор посвящен современным представлениям о клиническом течении гипофизитов, представлен набор характерных диагностических признаков заболевания по данным МРТ, также освещены рекомендуемые на сегодняшний день алгоритмы лечения. В статье обобщены данные зарубежной литературы и собственные клинические наблюдения с целью выработать оптимальный протокол МРТ-исследования у пациентов с подозрением на гипофизит, рекомендации для врачей-рентгенологов и эндокринологов для правильной интерпретации полученных результатов. Уникальностью данного обзора является отсутствие на сегодняшний день в российской литературе данных о клинической картине, диагностике и лечении гипофизита.
Ключевые слова
Для цитирования:
Воронцов А.В., Бабаева Д.М., Владимирова В.П., Дубовицкая Т.А., Гаврилова А.О., Белая Ж.Е., Мокрышева Н.Г. Клинико-рентгенологическая диагностика гипофизита: обзор литературы и собственные наблюдения. Проблемы Эндокринологии. 2022;68(2):16-33. https://doi.org/10.14341/probl12777
For citation:
Vorontsov A.V., Babaeva D.M., Vladimirova V.P., Dubovitskaya T.A., Gavrilova A.O., Belaya Zh.E., Mokryshevа N.G. Clinical and radiological diagnosis of hypophysitis: a review of literature and own data. Problems of Endocrinology. 2022;68(2):16-33. https://doi.org/10.14341/probl12777
ВВЕДЕНИЕ
Гипофизит — это редкое воспалительное заболевание гипофиза, характеризующееся неопухолевой инфильтрацией гипофиза, приводящее к нарушению его функций и увеличению объема. Его распространенность оценивается как 1 новый случай на 7–9 млн населения в год, на долю гипофизита приходится 0,24–0,88% всех заболеваний гипофиза [1].
Выделяют первичную (идиопатическую), которая возникает вследствие аутоиммунного воспаления непосредственно гипофиза, и вторичную, возникающую вследствие системных заболеваний или применения иммуномодулирующих лекарственных средств, формы гипофизита [1]. Вторичный гипофизит также может развиться на фоне образований хиазмально-селлярной области, таких как киста кармана Ратке, краниофарингиома, аденома, герминома [2–7]. В качестве системных заболеваний, приводящих к вторичному поражению гипофиза, выступают аутоиммунные (саркоидоз, гемохроматоз, гранулематоз Вегенера, болезнь Такаясу, болезнь Крона, гистиоцитоз из клеток Лангерганса и др.) или инфекционные заболевания (сифилис, туберкулез, грибковая и вирусная инфекция у пациентов с иммунодефицитом) [8–12].
Описано 5 гистологических вариантов первичного гипофизита: лимфоцитарный, гранулематозный, ксантоматозный, IgG4-ассоциированный (плазмоцитарный) и некротизирующий. Кроме того, описаны смешанные формы с одновременным сосуществованием гистологических признаков разных вариантов гипофизита [1–9][13].
В зависимости от распространенности воспалительного процесса, в соответствии с анатомическим строением гипофиза выделяют аденогипофизит (поражение передней доли гипофиза), инфундибулонейрогипофизит (поражение воронки и задней доли гипофиза), пангипофизит (поражение всего гипофиза). У женщин чаще встречается аденогипофизит, у мужчин и детей — инфундибулонейрогипофизит [1][4][7].
КЛИНИЧЕСКАЯ КАРТИНА
Для клинической картины гипофизита, вне зависимости от этиологии, ввиду увеличения объема гипофиза характерны головная боль и нарушение функции зрения вследствие компрессии хиазмы. В зависимости от степени вовлечения в воспалительный процесс гипофиза проявлением заболевания является нарушение его функций.
В 65% случаев поражается аденогипофиз, что приводит к парциальному или тотальному гипопитуитаризму. В отличие от других причин гипопитуитаризма, снижение продукции адренокортикотропного гормона (АКТГ) и тиреотропного гормона (ТТГ) очень часто развивается на ранних стадиях первичного гипофизита, что относит этих пациентов в группу повышенного риска развития жизнеугрожающей надпочечниковой недостаточности. Также могут возникать снижение продукции гонадотропинов, дефицит гормона роста, гиперпролактинемия. Реже, приблизительно в 10% всех случаев, развивается инфундибулонейрогипофизит, что сопряжено со снижением уровня вазопрессина с развитием несахарного диабета, иногда присоединяются признаки дефицита тропных гормонов.
Клинические признаки поражения переднего и заднего отделов гипофиза сосуществуют при пангипофизите, его частота составляет 25% (табл. 1) [9].
Таблица 1. Клинические признаки гипофизита в зависимости от объема поражения гипофиза
Table 1. Clinical signs of hypophysitis depending on the extent of the pituitary lesion
|
Симптомы гипофизита |
Аденогипофизит |
Инфундибулонейрогипофизит |
Пангипофизит |
|
Головная боль, % |
53 |
13 |
41 |
|
Нарушения зрения, % |
23 |
3 |
18 |
|
Гипокортицизм, % |
42 |
8 |
19 |
|
Гипотиреоз, % |
18 |
0 |
17 |
|
Гипогонадизм, % |
12 |
3 |
14 |
|
Гиперпролактинемия, % |
23 |
5 |
17 |
|
Несахарный диабет, % |
1 |
98 |
83 |
Примечание. Адаптировано из [9].
Первичный гипофизит
Лимфоцитарный гипофизит
Лимфоцитарное воспаление является наиболее распространенным гистологическим вариантом гипофизита — 68% случаев [4]. Впервые был описан в 1962 г. Goudie и Pinkerton. Чаще заболевают женщины, чем мужчины, с соотношением 3:1 [3], как правило, в четвертом десятилетии жизни. Лимфоцитарный гипофизит у большинства женщин был диагностирован на последнем месяце беременности и в послеродовом периоде, преимущественно в течение 2 мес после родов [3][12][14].
Гранулематозный гипофизит
Гранулематозный гипофизит впервые был описан Simmonds в 1917 г., который при гистологическом исследовании материалов 2000 гипофизов обнаружил 4 случая гранулематозного воспаления, не связанного с туберкулезом или сифилисом. Заболевание встречается крайне редко (около 20% диагностированных случаев), поражает мужчин и женщин в равных пропорциях. Гранулематозный гипофизит отличается от лимфоцитарного тем, что не ассоциирован с беременностью, спонтанно не разрешается и не протекает совместно с другими аутоиммунными заболеваниями. Этиология гранулематозного гипофизита неизвестна, при данном типе гипофизита необходимо исключить другие заболевания, связанные с образованиями гранулем (туберкулез, саркоидоз, гистиоцитоз), прежде чем рассматривать гранулематозное воспаление гипофиза как первичное [1][3][4].
Ксантоматозный гипофизит
Ксантоматозный гипофизит впервые описан в 1998 г., встречается реже, чем лимфоцитарный и гранулематозный (около 3% случаев) [4]. Считается, что этот вариант может быть спровоцирован воспалительной реакцией. Чаще регистрировался у женщин (3:1) на четвертом десятилетии их жизни.
Некротизирующий гипофизит
Наиболее редкий тип гипофизита — некротический, который был диагностирован у 4 пациентов в возрасте 12, 20, 33 и 39 лет (три случая были подтверждены гистологически). Наблюдался преимущественно у мужчин [1][3].
IgG4-ассоциированный гипофизит
IgG4-ассоциированный гипофизит часто развивается вследствие системных заболеваний, однако иногда выступает самостоятельным заболеванием. Чаще диагностируется у пожилых мужчин, для гистологической картины характерны плотная лимфоплазмоцитарная инфильтрация пораженной ткани гипофиза с преобладанием IgG4-позитивных плазматических клеток и фиброз на более поздних стадиях заболевания [1–2][15]. Клинически для IgG4-ассоциированного гипофизита характерны головная боль, сужение полей зрения, галакторея. Часто сопровождается поражением других органов (лимфатические узлы, поджелудочная железа, гепатобилиарный тракт, слюнные и слезные железы, забрюшинное пространство, аорта, перикард, щитовидная железа, легкие, почки, кожа, желудок, предстательная железа, яичники).
Диагноз IgG4-ассоциированного гипофизита подтверждается характерной гистологической картиной пунктата гипофиза. Однако биопсия гипофиза является инвазивной процедурой, и для установления диагноза могут быть использованы другие критерии, предложенные в 2011 г. Р. Leporati et al. (табл. 2) [16][17].
Таблица 2. Диагностические критерии IgG4-ассоциированного гипофизита
Table 2. Diagnostic criteria for IgG4-associated hypophysitis
|
Критерий 1 |
Гистологическая картина. Лимфоплазмоцитарная инфильтрация пораженной ткани гипофиза с более чем 10 IgG4-позитивными плазматическими клетками |
|
Критерий 2 |
МР-картина. Увеличение объема гипофиза и/или утолщенная воронка гипофиза |
|
Критерий 3 |
IgG4-ассоциированное заболевание другого органа, подтвержденное гистологически |
|
Критерий 4 |
Серологическое исследование крови. Повышенное содержание IgG4 в сыворотке крови (>140 мг/дл) |
|
Критерий 5 |
Терапевтический ответ на введение глюкокортикостероидов. Уменьшение объема гипофиза и улучшение клинических симптомов заболевания в ответ на терапию глюкокортикостероидами |
Примечание. Диагноз может быть установлен при выявлении 1 критерия,
при сочетании 2 и 3 критериев или 2, 4 и 5 критериев.
Вторичный гипофизит
Индуцированный иммуномодулирующей терапией
Ингибиторы контрольных иммунных точек — новый класс иммуноонкологических препаратов, широко используемых на данный момент в лечении онкологических заболеваний. Механизм действия связан с блокированием моноклональными антителами рецепторов CTLA 4 (ипилимумаб, тремелимумаб) и PD 1 (ниволумаб, пембролизумаб), Anti-PD1-L1 (авелумаб, дурвалумаб, атезолизумаб), что усиливает Т-клеточный противоопухолевый иммунный ответ и позволяет достичь положительного терапевтического эффекта в лечении злокачественных опухолей [1–4]. Тем не менее внешнее воздействие на иммунные контрольные точки может вызвать бесконтрольный иммунный ответ, что может способствовать развитию аутоиммунного поражения различных органов, в том числе гипофиза с развитием гипофизита.
Временной диапазон развития гипофизита от момента начала иммунопротивоопухолевой терапии варьирует в зависимости от используемого препарата, сообщалось, что он может развиться через несколько месяцев после начала иммунотерапии. Риск развития гипофизита при применении ипилимумаба наиболее высокий и, по-видимому, дозозависимый, более высокая распространенность отмечена у лиц, получающих 10 мг/кг, нежели 3 мг/кг. У пациентов, получающих сопутствующую цитотоксическую химиотерапию или радиотерапию головного мозга, риск развития гипофизита ниже, предположительно, за счет истощения иммунных клеток. Для клинической картины заболевания характерны такие неспецифические симптомы, как усталость, головная боль, миалгия, тошнота и симптомы дефицитов тропных гормонов, реже развиваются хиазмальный синдром и несахарный диабет. Могут появляться и такие более редкие симптомы, как спутанность сознания, галлюцинации, лабильное настроение, бессонница, анорексия, озноб [1][13][17][18].
Пациентам во время лечения ингибиторами контрольных иммунных точек рекомендованы наблюдение эндокринолога и проведение регулярного гормонального анализа крови. Приблизительно у 90% пациентов, у которых развивается гипофизит, отмечается дефицит АКТГ, зарегистрированы случаи фатальной острой надпочечниковой недостаточности, что подчеркивает важность оценки функции гипофиза до начала терапии и во время лечения, а также динамического наблюдения пациентов. Дефицит ТТГ также очень распространен (>80% пациентов). Предполагается, что снижение уровня ТТГ в сыворотке крови является ранним признаком индуцированного ингибиторами иммунных точек гипофизита.
Пациентам с подозрением на гипофизит показаны проведение МРТ гипофиза и осмотр офтальмолога с проведением периметрии обоих глаз для исключения сужения полей зрения. Faje A. в своем исследовании определил, что ~50% пациентов с гипофизитом имели диффузное увеличение гипофиза по данным МРТ до появления клинических симптомов [19][20].
Важно отметить, что высокие дозы глюкокортикостероидов не оказывают влияния на противоопухолевый эффект ингибиторов иммунных контрольных точек и лечение не должно быть отсрочено у пациентов с тяжелыми симптомами гипофизита с синдромом сдавления структур хиазмально-селлярной области. Лечение высокими дозами глюкокортикоидов, однако, не восстанавливает дефицит АКТГ, и большинству пациентов требуется долгосрочная заместительная терапия, когда в то же время дефицит ТТГ и гонадотропных гормонов часто восстанавливается. Решение о том, следует ли отказываться от иммуноонкологического лечения при возникновении такого осложнения, как гипофизит, должно быть взвешенно и принято в зависимости от конкретного клинического случая [1][3][4][7].
Гипофизит, связанный с образованиями хиазмальноселлярной области
Воспаление гипофиза может быть спровоцировано образованиями хиазмально-селлярной области. В таких случаях воспалительный инфильтрат в основном лимфоцитарный или ксантогранулематозный и фокусируется вокруг очага поражения, а не распространяется на всю железу.
- Герминома.
Герминома — редкая опухоль головного мозга, возникающая преимущественно у детей препубертатного возраста, в зарубежной литературе описаны единичные случаи возникновения вторичного гипофизита у детей с герминативно-клеточной опухолью [1].
- Киста кармана Ратке.
Разрыв кармана Ратке может вызывать гипофизит, проявляющийся сужением полей зрения, головной болью и гипопитуитаризмом, очень часто включая центральный несахарный диабет. Некоторые исследования показали, что многие случаи ксантоматозного гипофизита на самом деле могут быть связаны с разрывом кист кармана Ратке [1].
- Другие опухоли хиазмально-селлярной области.
Описаны случаи вторичного гипофизита в сочетании с краниофарингиомами, аденомами гипофиза [1][7]. В нашем примере представлена пациентка Б., 35 лет, с жалобами на прибавку массы тела, гипертензию и отечность, при выполнении МРТ-исследования диагностировалась аденома гипофиза в сочетании с утолщением и неоднородностью накопления контрастного вещества воронкой гипофиза
ДИАГНОСТИКА
Магнитно-резонансная томография
Золотым стандартом диагностики гипофизита является биопсия гипофиза с последующим гистологическим исследованием пунктата, однако, так как этот метод диагностики инвазивен, его применение ограничено. Так, при отсутствии показаний к хирургическому лечению диагноз гипофизита основывается на клинических, лабораторных и рентгенологических данных. МРТ является методом выбора при подозрении на гипофизит. Gutenberg A. еt al. рекомендуют использовать в протоколе МР-исследования режимы Т2-взвешенных и Т1-взвешенных изображений (ВИ) на дои постконтрастном корональных, сагиттальных и аксиальных изображениях (с толщиной среза до 3 мм) [8]. Диагностическими критериями гипофизита являются симметричное увеличение объема гипофиза (за счет увеличения размеров гипофиза) в сочетании с утолщением воронки гипофиза (в ряде случаев наблюдаются нормальные размеры воронки), диффузная неоднородность сигнала от ткани аденогипофиза и кистозные изменения структуры передней доли гипофиза разной степени выраженности, отсутствие типичного гиперинтенсивного МР-сигнала на Т1-взвешенных изображениях от задней доли гипофиза. Изменения воронки зависят от гистоморфологического вида гипофизита. По данным литературы, при лимфоцитарном и гранулематозном гипофизите происходит диффузное разрушение всего гипофиза, при этих вариантах на МРТ выявляются утолщение и неоднородность структуры воронки гипофиза. При ксантоматозном гипофизите может изменяться только передняя доля гипофиза, и при проведении МРТ воронка гипофиза у этих пациентов не изменена. В ряде случаев могут наблюдаться изменения структуры хиазмы и зрительных трактов (гиперинтенсивный МР-сигнал на Т2-ВИ от хиазмы и зрительных трактов) — при анализе данных литературы изменения хиазмы и зрительных трактов могут наблюдаться при гранулематозном (чаще) и лимфоцитарном гипофизите. В зависимости от вовлеченности в воспалительный процесс передней доли гипофиза, нейрогипофиза и стебля гипофиза разработана анатомическая классификация гипофизитов, согласно которой, гипофизит подразделяют на аденогипофизит, инфундибулонейрогипофизит и пангипофизит (рис. 1). При проведении МРТ с внутривенным контрастированием в активной фазе заболевания отмечается интенсивное и гетерогенное накопление контрастного препарата аденогипофизом (при всех вариантах гипофизита), характер накопления контрастного препарата воронкой зависит от типа гипофизита; также отмечается активное накопление контрастного препарата прилежащей твердой мозговой оболочкой с формированием «дурального хвоста» [5][21].

Рисунок 1. Схематичное изображение анатомических вариантов гипофизита. Слева: аденогипофизит с увеличением аденогипофиза с неизмененной воронкой гипофиза. В центре: пангипофизит с увеличением аденогипофиза и утолщением воронки гипофиза, с отсутствием типичного яркого сигнала от нейрогипофиза на Т1-ВИ. Справа: инфундибулонейрогипофизит с отсутствием яркого сигнала от нейрогипофиза на Т1-ВИ, утолщением воронки и треугольной деформацией гипофиза. (Chiloiro S. et al. Department of Endocrinology, School of Medicine, Catholic University of the Sacred Heart)
Figure 1. Schematic representation of the anatomical variants of hypophysitis. Left: adenohypophysitis with enlarged adenohypophysis with intact pituitary infundibulum. Center: panhypophysitis with enlargement of the adenohypophysis and thickening of the pituitary infundibulum, with no typical bright signal from the neurohypophysis on T1-WI. Right: infundibuloneurohypophysitis with no bright signal from the neurohypophysis on T1-WI, infundibulum thickening, and triangular deformity of the pituitary gland. (Chiloiro S. et al. Department of Endocrinology, School of Medicine, Catholic University of the Sacred Heart)
При подозрении на гипофизит результаты МРТ также позволяют провести дифференциальную диагностику и исключить у пациентов (всех возрастных категорий) аденому гипофиза, герминому и гистиоцитоз из клеток Лангерганса у подростков, краниофарингиому, кисту кармана Ратке и другие опухоли хиазмально-селлярной области и вторичные изменения гипоталамо-гипофизарной области, сопровождающиеся гипопитуитаризмом и несахарным диабетом [4][5].
Оценивая размеры гипофиза, мы основываемся на собственном опыте, согласно нашим данным, у 99% здоровых людей вертикальный размер гипофиза не превышает 8–8,5 мм, что, по нашему мнению, позволяет считать именно данный размер верхней границей нормы [5]. Сагиттальный и поперечный размеры в большинстве случаев определяются размерами турецкого седла. Толщина воронки вариабельна, чаще всего она находится в пределах 1–3 мм, с возможными колебаниями в дистальной и проксимальной части.
К диагностическим критериям гипофизита также можно отнести результаты динамического наблюдения, на фоне лечения (кортикостероидами) отмечается довольно быстрое уменьшение размеров гипофиза и воронки (в ряде случаев временное, с последующим рецидивом в виде увеличения объема гипофиза). В отдаленные сроки заболевания могут наблюдаться атрофия аденогипофиза с формированием пустого турецкого седла, фиброзные изменения структуры аденогипофиза. Отсутствие гиперинтенсивного на Т1-ВИ сигнала от задней доли гипофиза чаще сохраняется и в отдаленный период. При динамическом наблюдении также изменяются результаты МРТ-исследования с контрастным усилением, отмечается субтотальное/тотальное снижение накопления контрастного препарата аденогипофизом, вплоть до участков отсутствия контрастирования, что объясняется наличием участков фиброза в структуре аденогипофиза [4][5][22].
В 2009 г. была предпринята попытка объективизировать, систематизировать диагностические критерии гипофизита по результатам МРТ с целью более точной дифференциальной диагностики гипофизита и аденомы гипофиза и в конечном счете избежать необоснованного хирургического вмешательства. В результате были определены 8 основных предикторов, позволяющих провести дифференциальную диагностику. К ним относились возраст пациента, у женщин наличие беременности, объем гипофиза, характер и скорость накопления контрастного препарата, симметричность увеличения гипофиза, визуализация нейрогипофиза, изменения воронки гипофиза, изменение слизистой оболочки в пазухах основной кости и/или прилегающих ячейках решетчатой кости. Результаты МРТ предлагалось оценивать по балльной системе. Данный подход не нашел широкого применения [5].
В нашем Центре мы также учитываем совокупность признаков, характерных для гипофизита (описанных ранее), и с учетом клинико-лабораторных данных считаем правомочным диагностировать гипофизит по данным МРТ.
Гипофизит должен быть заподозрен у пациентов с нарушением функции гипофиза и/или неврологическими (головная боль), офтальмологическими нарушениями (сужение полей зрения) при типичных МРТ-признаках поражения гипофиза. Гипофизит обычно диагностируют во время острой фазы, когда происходят увеличение гипофиза и утолщение воронки вследствие воспалительного инфильтрата, манифестируют признаки и симптомы заболевания. Хроническая же фаза гипофизита характеризуется необратимым гипопитуитаризмом, обусловленным развитием фиброза гипофиза и впоследствии синдрома «пустого» турецкого седла [4][5] (рис. 2–5).

Рисунок 2. Пациентка К., 36 лет. Лимфоцитарный гипофизит. Первичная МРТ от 2014 г. по поводу галактореи и головной боли: а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т1-ВИ, постконтрастный корональный срез; г) Т1-ВИ, постконтрастный сагиттальный срез. Выявлены увеличение и диффузная неоднородность структуры гипофиза, утолщение воронки, с диффузным и неоднородным накоплением контрастного вещества.
Figure 2. Patient K., 36 years old. Lymphocytic hypophysitis. Primary MRI from 2014 for galactorrhea and headache: a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T1-WI, postcontrast coronal section; d) T1-WI, post-contrast sagittal section. An increase and diffuse heterogeneity of the structure of the pituitary gland, thickening of the infundibulum, with diffuse and heterogeneous accumulation of a contrast agent were revealed.
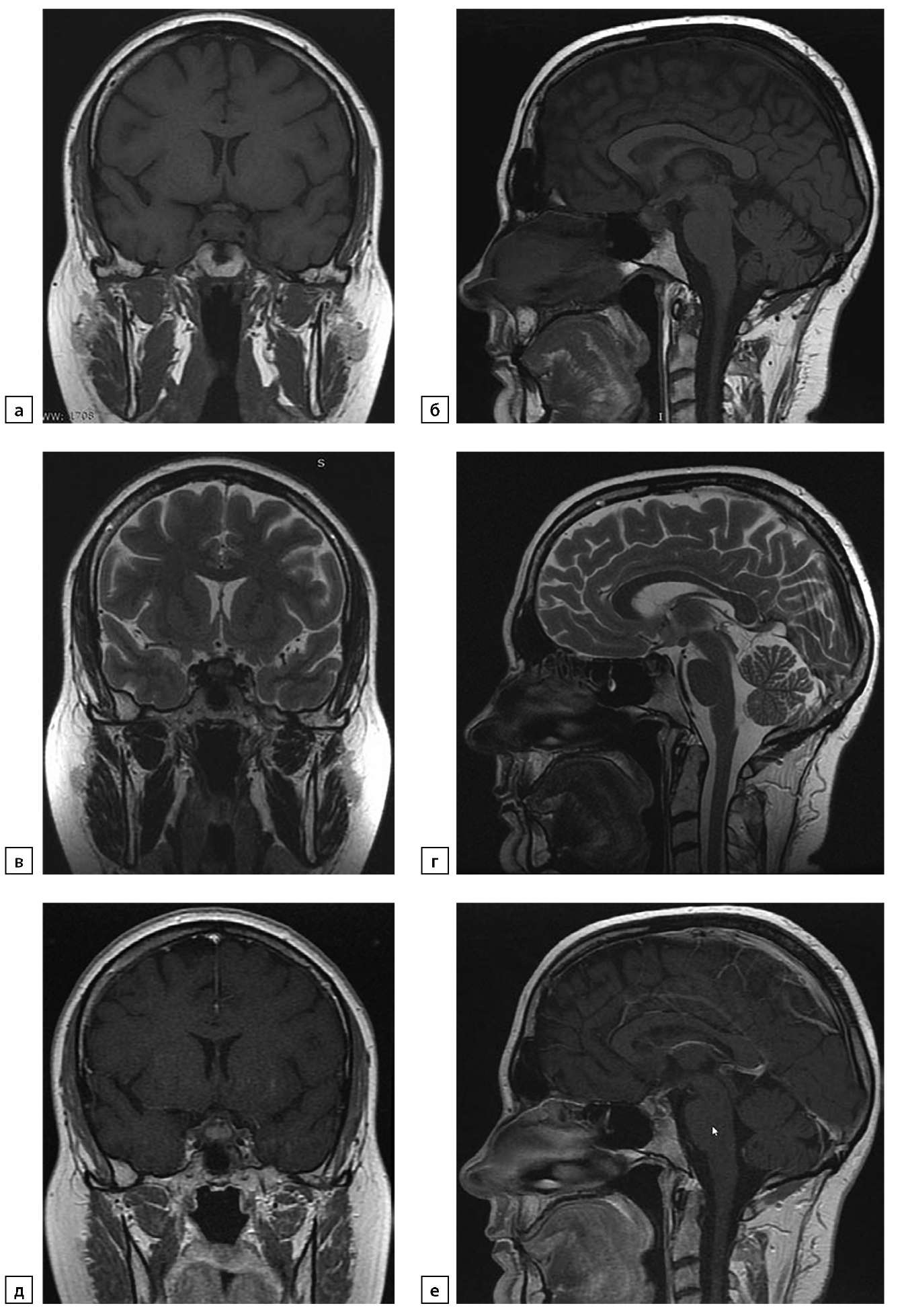
Рисунок 3. Та же пациентка. МРТ от 2019 г. после гистологической верификации: а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т2-ВИ, сагиттальный срез; д) Т1-ВИ, постконтрастный корональный срез; е) Т1-ВИ, постконтрастный сагиттальный срез. Выявлены более выраженное увеличение и неоднородность структуры гипофиза, в том числе за счет формирования фиброзных изменений и компрессии хиазмы.
Figure 3. The same patient. MRI from 2019 after histological verification: a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T2-WI, sagittal section; e) T1-WI, postcontrast coronal section; f) T1-WI, post-contrast sagittal section. A more pronounced increase and heterogeneity of the structure of the pituitary gland were revealed, including due to the formation of fibrous changes and compression of the chiasm.
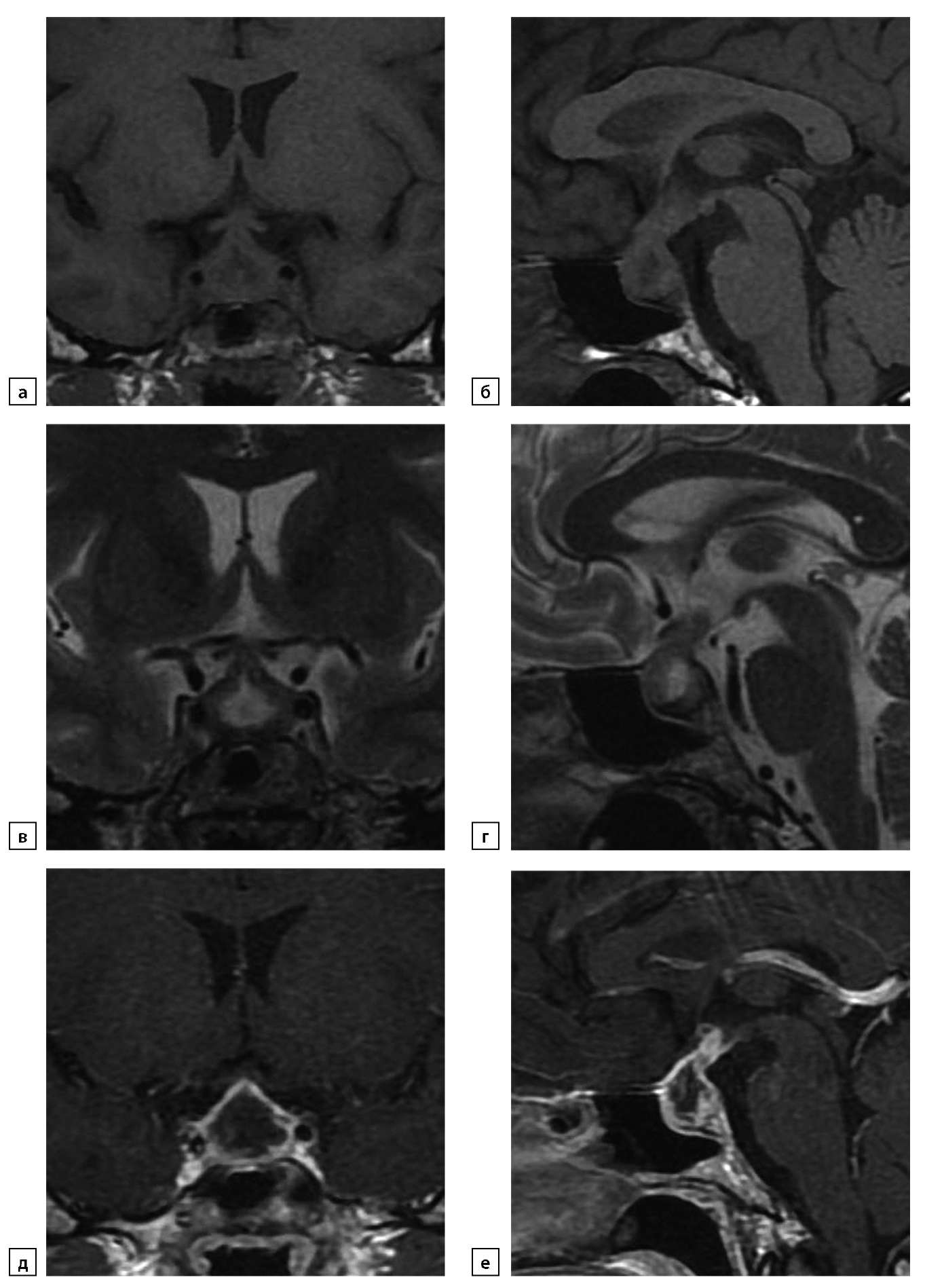
Рисунок 4. Пациентка Е., 38 лет. Лимфоцитарный гипофизит. Жалобы на выраженные головные боли, нарушение менструации, онемение правой половины лица. По данным МРТ от 24.06.2019: а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т2-ВИ, сагиттальный срез; д) Т1-ВИ, постконтрастный корональный срез; е) Т1-ВИ, постконтрастный сагиттальный срез. Гипофиз деформирован, имеет выпуклый верхний контур, структура его неоднородна, в центральной части определяется жидкостной компонент размерами 5х7х5,5 мм (инфундибулогипофизит); интенсивное контрастирование определяется по периферии гипофиза. Воронка деформирована, равномерно утолщена до 4,5 мм, неоднородно интенсивно накапливает контрастный препарат. Типичный сигнал от задней доли гипофиза не определяется. Супраселлярная цистерна сужена.
Figure 4. Patient E., 38 years old. Lymphocytic hypophysitis. Complaints of severe headaches, menstruation disorders, numbness of the right half of the face. According to MRI data from 06/24/2019: a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T2-WI, sagittal section; e) T1-WI, postcontrast coronal section; f) T1-WI, post-contrast sagittal section. The pituitary gland is deformed, has a convex upper contour, its structure is heterogeneous, in the central part there is a liquid component measuring 5x7x5.5 mm (infundibulohypophysitis); intensive contrasting is determined by the periphery of the pituitary gland. The funnel is deformed, evenly thickened up to 4.5 mm, and the contrast agent accumulates non-uniformly intensively. A typical signal from the posterior pituitary is not detected. The suprasellar cistern is narrowed.
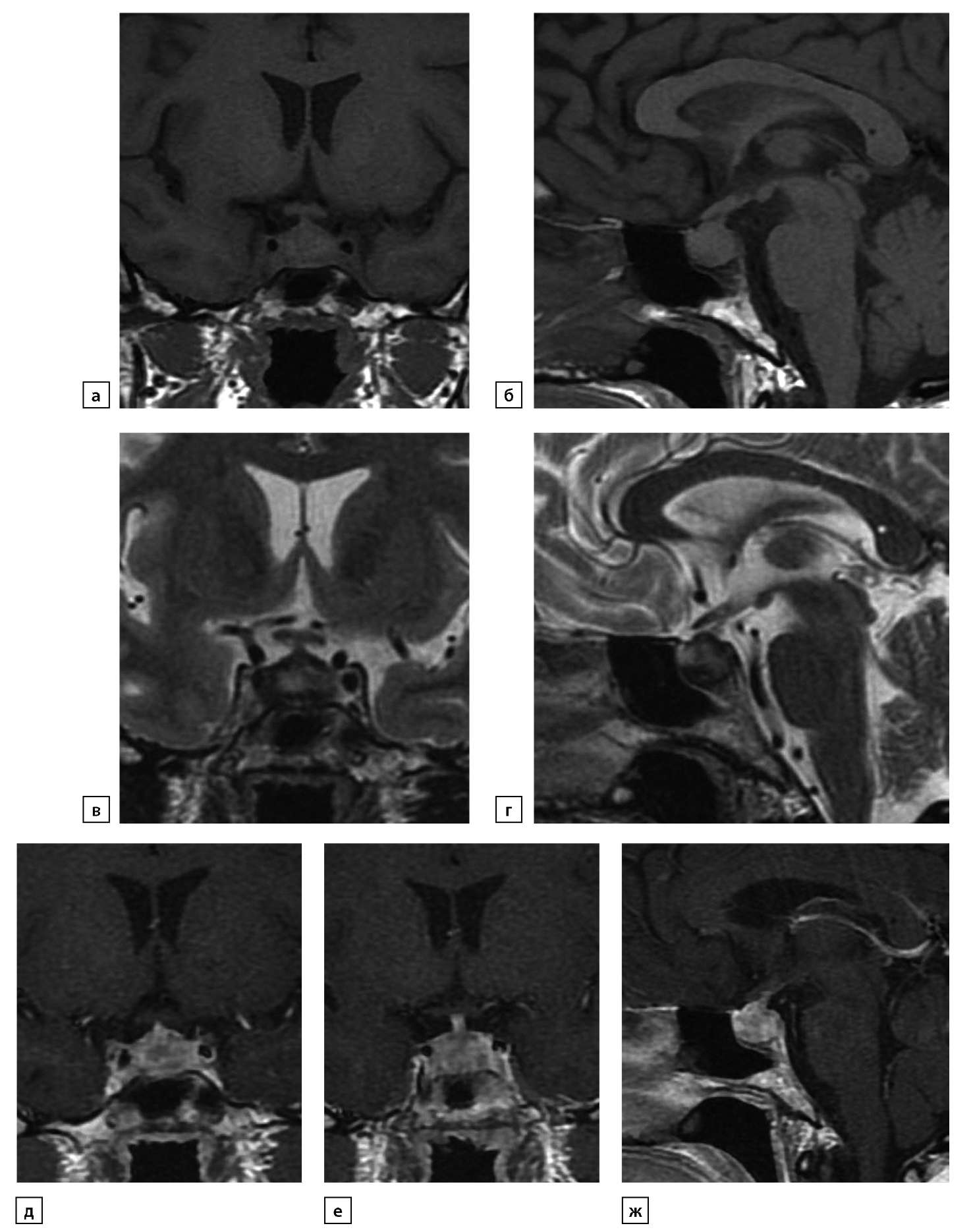
Рисунок 5. Та же пациентка. По данным МРТ в динамике от 24.09.2019 на фоне терапии глюкокортикостероидами в больших дозах: а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т2-ВИ, сагиттальный срез; д) Т1-ВИ, постконтрастный корональный срез; е) Т1-ВИ, постконтрастный корональный срез; ж) Т1-ВИ, постконтрастный сагиттальный срез. Гипофиз увеличен, деформирован, имеет выпуклый верхний контур, структура его неоднородна, при контрастном усилении отмечается интенсивное, неоднородное накопление контрастного препарата. Воронка деформирована, утолщена преимущественно в дистальной части (до 3,5 мм), однородно интенсивно накапливает контрастный препарат. Типичный сигнал от задней доли гипофиза не определяется. Супраселлярная цистерна сужена, расстояние до хиазмы 1 мм. Отмечается активное накопление контрастного препарата диафрагмой турецкого седла. По сравнению с предыдущим исследованием от 24.06.2019 отмечается уменьшение размеров гипофиза.
Figure 5. The same patient. According to MRI data in dynamics from 09/24/2019 against the background of high-dose glucocorticosteroid therapy: a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T2-WI, sagittal section; e) T1-WI, post-contrast coronal cut; f) T1-WI, post-contrast coronal section; g) T1-WI, post-contrast sagittal section. The pituitary gland is enlarged, deformed, has a convex upper contour, its structure is heterogeneous, with contrast enhancement there is an intense, heterogeneous accumulation of the contrast agent. The funnel is deformed, thickened mainly in the distal part (up to 3.5 mm), uniformly intensively accumulates a contrast agent. A typical signal from the posterior pituitary is not detected. The suprasellar cistern is narrowed, the distance to the chiasma is 1 mm. There is an active accumulation of the contrast agent by the diaphragm of the Turkish saddle. Compared to the previous study dated 06/24/2019, there is avdecrease in the size of the pituitary gland.
Лабораторная диагностика
Аутоиммунная этиология первичного гипофизита обусловлена наличием антител к гипофизу, в качестве мишеней для аутоиммунной агрессии рассматриваются следующие антигены: α-енолаза, гормон роста, специфичные для гипофиза факторы 1a и 2 (PGSF1a и PGSF2), регуляторные ферменты, продуцируемые в гипофизе (PC1/3, PC2, CPE и 7B2), секретогранин II, открытая рамка считывания хромосом 14 (C14orf166), специфичный фактор транскрипции TPIT и хорионический соматомаммотрофин (HCS). Для выявления антител к гипофизу при первичном гипофизите использовали несколько методик (иммуноферментный анализ, радиолигандный анализ, иммуноблоттинг и иммунофлюоресценцию), причем распространенность антителоположительного гипофизита составляет 11–73% в зависимости от тестируемого антигена(ов) и используемой методики. Однако роль этих антител неясна, и они не специфичны для гипофизита. Например, антитела к гипофизу были идентифицированы методом непрямой иммунофлюоресценции у ~45% пациентов с гипофизитом, подтвержденным гистологически, но также были обнаружены в сыворотке крови у пациентов с изолированным центральным несахарным диабетом (35%), герминомами (33%), недостаточностью тропных гормонов, продуцируемых аденогипофизом (29%), пролактиномами (27%), кистами кармана Ратке (25%), краниофарингиомами (17%), гормонально-неактивными образованиями гипофиза (13%), соматотропиномами (12%) и у здоровых людей (5%). Они также могут быть обнаружены у пациентов с другой аутоиммунной патологией, особенно при хроническом аутоиммунном тиреоидите [23][24].
Клинический случай
Пациент З., 56 лет, в 2017 г. поступил в стационар с жалобами на выраженную головную боль, сухость кожи, снижение веса, потерю аппетита. По данным проведенного обследования был выявлен пангипопитуитаризм: вторичный гипотиреоз (ТТГ – 0,32 мМЕ (0,4–4,2), свободный тироксин — 4,3 пмоль/л (7,86–14,4)), вторичный гипогонадизм (фолликулостимулирующий гормон — 1,81 Ед/л (1,6–9,7), лютеинизирующий гормон — 0,591 Ед/л (2,5–11), тестостерон — 0,773 нмоль/л (11–33,5)), вторичный гипокортицизм (кортизол утром — 100,5 нмоль/л (123–626), АКТГ — 22,51 пг/мл (7–66)), несахарный диабет. Было проведено МРТ-исследование головного мозга, по результатам которого выявлено инфильтративное поражение гипофиза, характерное для гипофизита (рис. 6). В качестве лечения пангипопитуитаризма была назначена заместительная терапия левотироксином натрия, десмопрессином и глюкокортикостероидами.
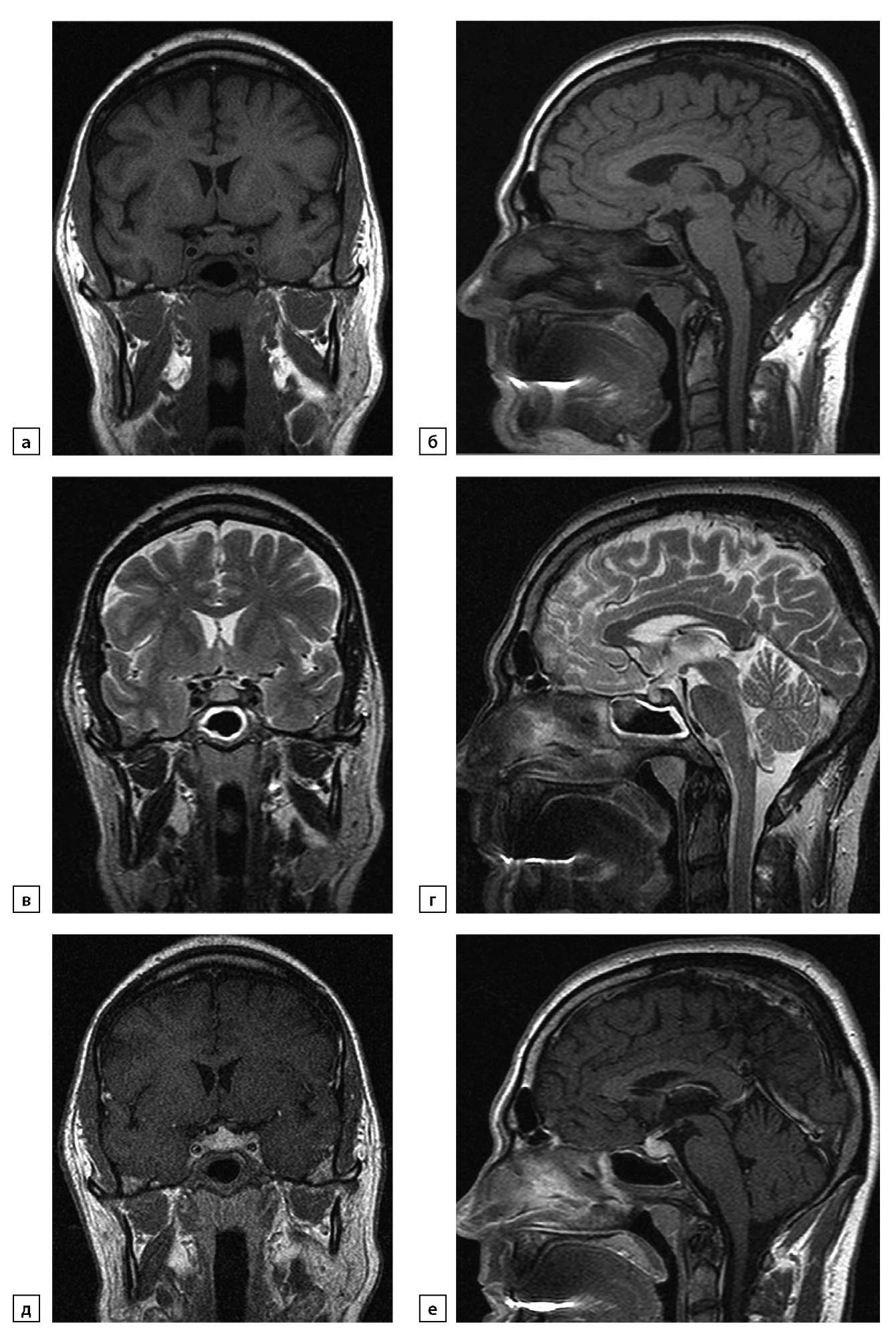
Рисунок 6. а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т2-ВИ, сагиттальный срез; д) Т1-ВИ, постконтрастный корональный срез; е) Т1-ВИ, постконтрастный сагиттальный срез. Определяются увеличение размеров и деформация гипофиза, воронка смещена кпереди, толщиной 3,5 мм. При контрастном усилении отмечается выраженная неоднородность накопления контрастного вещества гипофизом
Figure 6. a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T2-WI, sagittal section; e) T1-WI, postcontrast coronal section; f) T1-WI, post-contrast sagittal section. An increase in size and deformation of the pituitary gland are determined, the funnel is displaced anteriorly, 3.5 mm thick. With contrast enhancement, there is a pronounced heterogeneity of the accumulation of the contrast agent by the pituitary gland.
Для дифференциальной диагностики с герминомой был рекомендован анализ крови на β-субъединицу хорионического гонадотропина человека (β-ХГЧ) и α-фетопротеин.
По данным исследований от 21.06.2017: β-ХГЧ св. менее 2 нг/мл (норма менее 2,0), α-фетопротеин 1,87 МЕ/мл (менее 7,29). Гистиоцитоз исключен по КТ легких и черепа.
В стационаре пациенту проводилась пульс-терапия метилпреднизолоном по поводу гипофизита, в суммарной дозе метилпреднизолона 12 г. После проведенного лечения по данным МРТ головного мозга отмечено уменьшение размеров гипофиза по сравнению с предыдущим МРТ-исследованием с уменьшением толщины воронки гипофиза (рис. 7). Пациент отметил улучшение состояния в виде снижения выраженности головных болей.

Рисунок 7. а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т2-ВИ, сагиттальный срез; д) Т1-ВИ, постконтрастный корональный срез; е) Т1-ВИ, постконтрастный сагиттальный срез. Определяются уменьшение вертикального размера гипофиза и изменение структуры.
Figure 7. a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T2-WI, sagittal section; e) T1-WI, postcontrast coronal section; f) T1-WI, post-contrast sagittal section. A decrease in the vertical size of the pituitary gland and a change in structure are determined.
Однако спустя 2 нед цефалгический синдром рецидивировал, по поводу чего пациентом был начат самостоятельный прием дексаметазона 2–4 мг/сут с положительным эффектом. 17.11.2017 была проведена трансназальная транссфеноидальная гипофизэктомия с применением эндоскопического ассистирования по поводу гипофизита, по результатам гистологического исследования подтвержден диагноз лимфоцитарного гипофизита: фрагмент аденогипофиза с участками атрофии, фиброза, очаговой лимфоплазмоцитарной инфильтрации стромы с примесью нейтрофилов и эозинофилов, отдельно расположены 2 мелких фрагмента гиалинизированной соединительной ткани с обильной лимфоидной инфильтрацией; 3 мелких фрагмента аденогипофиза с признаками атрофии, фиброза, обильной лимфоплазмоцитарной инфильтрации стромы.
После оперативного лечения по данным МРТ-исследования головного мозга: состояние после гипофизэктомии, «пустое» турецкое седло (рис. 8).

Рисунок 8. а) Т2-ВИ, корональный срез; б) Т2-ВИ, сагиттальный срез; в) Т1-ВИ, постконтрастный корональный срез; г) Т1-ВИ, постконтрастный сагиттальный срез. Супраселлярная цистерна пролабирует в полость турецкого седла. На фоне послеоперационных изменений гипофиз уплощен, деформирован, воронка не утолщена. Типичный МРТ-сигнал от нейрогипофиза не определяется.
Figure 8. a) T2-WI, coronal section; b) T2-WI, sagittal section; c) T1-WI, postcontrast coronal section; d) T1-WI, post-contrast sagittal section. The suprasellar cistern protrudes into the cavity of the Turkish saddle. Against the background of postoperative changes, the pituitary gland is flattened, deformed, the infundibulum is not thickened. A typical MRI signal from the neurohypophysis is not detected.
В апреле 2018 г. — рецидив выраженных головных болей, в это время получал следующую заместительную терапию: левотироксин натрия 100 мкг в сутки, десмопрессин 30 мкг на ночь (нерегулярно из-за усиления головных болей). Кроме того, пациент продолжал получать дексаметазон 2 мг в/м 1 раз в 1–2 дня. Офтальмологом диагностирована нейропатия блокового нерва справа. Во время госпитализации дексаметазон был заменен на метилпреднизолон 8 мг/сут, на фоне чего цефалгический синдром снова был купирован. Была проведена МРТ головного мозга, выявлена дополнительная ткань в правом кавернозном синусе, утолщение намета мозжечка справа (отрицательная динамика) — объемный процесс твердой мозговой оболочки (рис. 9).
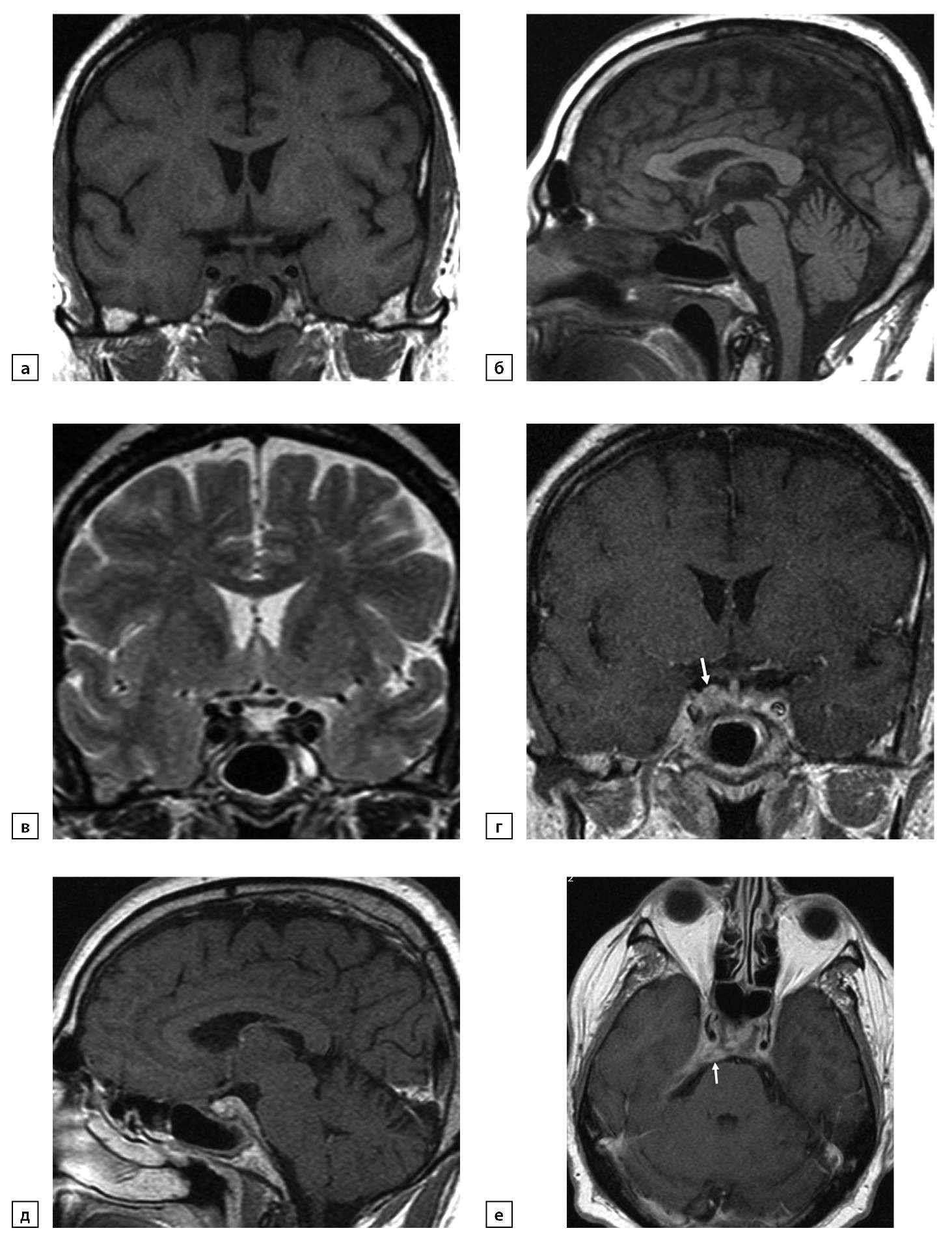
Рисунок 9. а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т1-ВИ, постконтрастный корональный срез; д) Т1-ВИ, постконтрастный сагиттальный срез; е) Т1-ВИ, постконтрастный аксиальный срез. Отмечаются послеоперационные изменения структуры гипофиза, на фоне которых в правом кавернозном синусе и в области крыла клиновидной кости определяется дополнительная ткань, при контрастном усилении активно накапливающая контрастный препарат, выявляется связь образования с утолщенным наметом мозжечка (также активно накапливающим контрастный препарат) и с оболочкой межножковой цистерны (стрелка)
Figure 9. a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T1-WI, postcontrast coronal section; e) T1-WI, post-contrast sagittal section; f) T1-WI, post-contrast axial section. Postoperative changes in the structure of the pituitary gland are noted, against the background of which additional tissue is determined in the right cavernous sinus and in the region of the wing of the sphenoid bone, with contrast enhancement actively accumulating the contrast agent, a connection between the formation and the thickened cerebellar tentorium (also actively accumulating cont. herbal preparation) and with a shell of the interpeduncular cistern (arrow)
В связи с вторичным гипогонадизмом 25.07.18 г. после определения уровня простат-специфического антигена (0,2 нг/мл) выполнена инъекция тестостерона ундеканоата 1000 мг. В сентябре и декабре 2018 г. проведены вторая и третья инъекции тестостерона ундеканоата. На контрольном МРТ-исследовании через 6 мес отметилась положительная динамика в виде уменьшения размеров дополнительной ткани в правом кавернозном синусе (рис. 10).

Рисунок 10. а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т2-ВИ, корональный срез; г) Т1-ВИ, постконтрастный корональный срез; д) Т1-ВИ, постконтрастный сагиттальный срез; е) Т1-ВИ, постконтрастный аксиальный срез. Отмечается утолщение твердой мозговой оболочки в области правого кавернозного синуса, в области крыла клиновидной кости, при контрастном усилении патологического накопления контрастного препарата не выявлено (стрелка)
Figure 10. a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T2-WI, coronal section; d) T1-WI, postcontrast coronal section; e) T1-WI, post-contrast sagittal section; f) T1-WI, post-contrast axial section. There is a thickening of the dura mater in the region of the right cavernous sinus, in the region of the wing of the sphenoid bone, with contrast enhancement, no pathological accumulation of the contrast agent was detected (arrow)
Данный клинический случай подчеркивает тот факт, что хирургическое лечение должно проводиться по показаниям.
По итогам проведенного лечения состояние пациента З. удовлетворительное, активных жалоб не предъявляет, получает заместительную терапию по поводу пангипопитуитаризма, по данным МРТ — без динамики, офтальмологом данных за нейропатию не получено, нарушения периферических полей зрения не выявлено.
ДИФФЕРЕНЦИАЛЬНАЯ ДИАГНОСТИКА
В первую очередь следует отметить, что для правильной интерпретации структурных изменений хиазмально-селлярной области необходим учет клинической картины, результатов гормонального и рентгенологических исследований. Так, герминомы, возникающие в хиазмально-селлярной области, трудно дифференцировать от гипофизита у детей из-за сходных клинических особенностей (несахарный диабет + преждевременное половое развитие + дефицит гормона роста + сужение полей зрения). Важность правильной диагностики заключается в принципиально разном лечении и исходе заболевания. Доказанные биопсией случаи первичного гипофизита крайне редки у детей и подростков, поэтому у детей младше 10 лет герминома должна рассматриваться как наиболее вероятный диагноз. Опухолевые маркеры, такие как α-фетопротеин, β-человеческий хорионический гонадотропин или плацентарная щелочная фосфатаза в спинномозговой жидкости, могут являться ценными диагностическими критериями для диагностики герминомы. Однако биопсия гипофиза остается золотым стандартом диагностики.
Следует отметить, что гипопитуитаризм, являющийся общим проявлением гипофизита и герминомы, может возникать задолго до того, как герминома будет визуализироваться на МРТ.
Необходимо проводить дифференциальную диагностику гипофизита с аденомой гипофиза и синдромом Шихана у пациенток в послеродовом периоде.
По гормональному исследованию крови у пациентов с аденомами можно обнаружить дефицит гонадотропинов, ТТГ и АКТГ, как и при гипофизите, однако следует иметь в виду, что при гипофизите надпочечниковая недостаточность является самым ранним проявлением, затем развиваются вторичный гипотиреоз и гипогонадотропный гипогонадизм, уровень соматотропного гормона (СТГ) снижается редко. Некоторые авторы предлагают проводить тест с агонистами дофамина при дифференциальной диагностике гипофизита и пролактином, в последнем случае обнаруживается уменьшение размеров опухоли при отсутствии подобного эффекта у пациентов с гипофизитом. На МРТ аденома гипофиза очень часто проявляется асимметричным увеличением гипофиза, иногда отклонением неизмененной воронки, редко могут распространяться в кавернозный синус, типичный сигнал на Т1-ВИ от нейрогипофиза всегда присутствует, а при контрастном усилении аденома гипофиза характеризуется сниженным, замедленным накоплением контрастного вещества очагом, в то время как остальная часть аденогипофиза остается неизмененной [1][5][8].
Общим для гипофизита и синдрома Шихана является то, что они часто наблюдаются в послеродовом периоде. Синдром Шихана — это ишемический некроз гипофиза и его стойкая гипофункция вследствие послеродового кровотечения. Это осложнение родов со значительной кровопотерей также называют послеродовым гипопитуитаризмом [5][17]. Главным отличием на МРТ от гипофизита при синдроме Шихана является увеличение размеров гипофиза на фоне геморрагических изменений; также может присутствовать отек зрительных трактов или хиазмы [5][18]. Первые симптомы гипофизита появляются преимущественно на поздних сроках беременности, в то время как синдром Шихана развивается в послеродовом периоде. Кроме того, при синдроме Шихана отсутствует лактация в послеродовом периоде, что довольно редко встречается при лимфоцитарном гипофизите. Развитие симптома «пустого» турецкого седла на МРТ при синдроме Шихана может возникнуть в долгосрочной перспективе [12][14].
В целом дифференциальная диагностика может быть затруднительна ввиду схожих проявлений заболеваний. Обязательным диагностическим методом является выполнение МРТ с внутривенным контрастированием всем пациентам с подозрением на гипофизит (рис. 11) [13][14].

Рисунок 11. Пациентка Б., 35 лет, с жалобами на головную боль, прибавку в весе, нечеткость зрения, жажду. Вторичный гипофизит на фоне АКТГ-продуцирующей аденомы гипофиза. По данным МРТ: а) Т1-ВИ, корональный срез; б) Т1-ВИ, сагиттальный срез; в) Т1-ВИ, постконтрастный корональный срез; г) Т1-ВИ, постконтрастный сагиттальный срез. Определяется утолщение воронки (стрелка), при контрастном усилении отмечаются неоднородность накопления контрастного вещества воронкой гипофиза и наличие в структуре аденогипофиза аденомы (пунктирная стрелка)
Figure 11. Patient B., 35 years old, complaining of headache, weight gain, blurred vision, thirst. Secondary hypophysitis on the background of ACTH-producing pituitary adenoma. According to MRI: a) T1-WI, coronal section; b) T1-WI, sagittal section; c) T1-WI, postcontrast coronal section; d) T1-WI, post-contrast sagittal section. Thickening of the funnel is determined (arrow), with contrast enhancement, heterogeneity of the accumulation of the contrast agent by the funnel of the pituitary gland and the presence of an adenoma in the structure of the adenohypophysis are noted (dotted arrow)
ЛЕЧЕНИЕ
Лечение гипофизита должно быть направлено на уменьшение воспаления и объема гипофиза и на восполнение имеющегося гормонального дефицита, возникшего вследствие нарушения функций гипофиза.
В качестве иммуносупрессивной терапии применяют глюкокортикостероиды и цитостатики. Иммуносупрессивную терапию следует назначать только во время острой фазы гипофизита с целью уменьшения воспаления и объема гипофиза и, как следствие, во избежание прогрессирования клинических симптомов. Глюкокортикостероиды рассматриваются как препараты 1-й линии в качестве иммуносупрессивной терапии [1][3][4][25].
На данный момент не существует протоколов ведения больных с гипофизитами, отсутствуют однозначные рекомендации по дозам глюкокортикостероидов и продолжительности терапии.
Положительный терапевтический эффект иммуносупрессивной глюкокортикоидной терапии описан в 15–41% случаев первичного гипофизита и в 42–64% случаев гипофизита вследствие приема иммуномодулирующих препаратов.
Зарегистрированы случаи восстановления секреции гонадотропинов, ТТГ, СТГ, функции нейрогипофиза вследствие иммуносупрессивной терапии глюкокортикостероидами. Однако рецидив заболевания может наблюдаться до 38% случаев после глюкокортикоидной иммуносупрессивной терапии.
В случаях резистентности к глюкокортикоcтероидам и при возникновении признаков экзогенного гиперкортицизма успешно применяются цитостатики, такие как азатиоприн, метотрексат и циклоспорин. Однако оценить отсроченный терапевтический эффект сложно [10][11].
У больных с вторичным гипотиреозом заместительную терапию следует назначать только после коррекции гипокортицизма, в обратном случае может возникнуть аддисонический криз в условиях декомпенсации надпочечниковой недостаточности [11]. В отношении гипогонадотропного гипогонадизма и дефицита СТГ назначение заместительной терапии не показано в острую фазу заболевания, она может быть отсрочена до хронической фазы заболевания после глюкокортикоидной иммуносупрессивной терапии [12]. Было описано возможное разрешение этих тропных дефицитов после глюкокортикоидной иммуносупрессивной терапии [13]. У пациентов с гипофизитом вследствие иммуномодулирующей терапии заместительная терапия гипогонадизма должна назначаться в зависимости от типа неоплазии, препараты рекомбинантного человеческого гормона роста противопоказаны [1][12][25].
Хирургическое лечение показано в случаях, сопровождающихся сужением полей зрения, снижением остроты зрения, параличом черепных нервов, отсутствием положительного терапевтического эффекта от медикаментозной терапии. Хирургическое лечение позволяет устранить компрессию гипофиза на структуры хиазмально-селлярной области, однако наблюдался рецидив заболевания у 25% пациентов при динамическом наблюдении в течение 3 лет. Функция гипофиза улучшилась только у 8% пациентов после операции, нивелирование хиазмального синдрома также отражается низким процентов случаев [25][26].
Стереотаксическая лучевая терапия (радиохирургия) была эффективно применена у нескольких пациентов с рецидивами лимфоцитарного гипофизита [1][23].
ДИНАМИЧЕСКОЕ НАБЛЮДЕНИЕ ПАЦИЕНТОВ
У пациентов в острой фазе гипофизита рекомендуется оценивать гипофизарную функцию и адекватность заместительной терапии ежемесячно. Повторное проведение МРТ гипофиза рекомендовано через 3 мес после постановки диагноза, далее — каждые 6 мес. В случае гипофизита, вследствие применения иммуномодулирующих препаратов с неврологическими симптомами, рекомендовано проведение МРТ гипофиза ежемесячно. В хронической фазе гипофизита следует проводить МРТ гипофиза при появлении симптомов, указывающих на рецидив заболевания [11].
ЗАКЛЮЧЕНИЕ
В настоящее время нет общепринятых алгоритмов для диагностики и ведения больных с гипофизитом. Несмотря на то что гипофизит в последнее время выявляется чаще, диагностика заболевания остается сложной задачей. Трудности диагностики гипофизитов обусловлены многообразием диагнозов со схожими клиническими симптомами и гормональными нарушениями, отсутствием однозначных рентгенологических паттернов. Гормональные и рентгенологические исследования в динамике упрощают диагностику гипофизитов, делая ее более очевидной для клиницистов и рентгенологов. Мы рекомендуем проведение МРТ-исследования головного мозга с контрастным усилением всем пациентам с некупируемым нестероидными противовоспалительными средствами цефалгическим синдромом и нарушением гормонального статуса в наиболее ранние сроки в связи с разнообразными вариантами гипофизита и изменением структуры гипофиза при динамическом наблюдении. В данной статье проиллюстрированы основные рентгенологические варианты гипофизита с приведением клинического случая пациента с некупируемой головной болью. На основании наших данных мы рекомендуем повторное проведение МРТ головного мозга с контрастным усилением в динамике через 3 мес с подозрением на гипофизит. Своевременная диагностика гипофизита позволит избежать необоснованного нейрохирургического лечения.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с публикацией настоящей статьи.
Участие авторов. Воронцов А.В. — концепция и дизайн статьи, анализ литературы, написание статьи, утверждение итогового варианта текста рукописи; Бабаева Д.М. — концепция и дизайн статьи, анализ литературы, написание статьи, утверждение итогового варианта текста рукописи; Владимирова В.П. — концепция и дизайн статьи, анализ литературы, написание статьи, утверждение итогового варианта текста рукописи; Дубовицкая Т.А. — концепция и дизайн статьи, анализ литературы, написание статьи, утверждение итогового варианта текста рукописи; Гаврилова А.О. — концепция и дизайн статьи, анализ литературы, редактирование текста, написание статьи, утверждение итогового варианта текста рукописи; Белая Ж.Е. — редактирование текста, утверждение итогового варианта текста рукописи; Мокрышева Н.Г. — редактирование текста; утверждение итогового варианта текста рукописи. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Согласие пациента. Пациенты добровольно подписали информированное согласие на публикацию персональной медицинской информации в обезличенной форме (именно в этом журнале).
Список литературы
1. Kluczyński Ł, Gilis-Januszewska A, Rogoziński D, et al. Hypophysitis — new insights into diagnosis and treatment. Endokrynol Pol. 2019;70(3):260-269. doi: https://doi.org/10.5603/EP.a2019.0015.
2. Юкина М.Ю., Трошина Е.А., Платонова Н.М., Нуралиева Н.Ф. Аутоиммунная IgG4-ассоциированная эндокринная патология // Ожирение и метаболизм. — 2017. — Т. 14. — №3. — С. 43-47. doi: https://doi.org/10.14341/omet2017343-47
3. Joshi MN, Whitelaw BC, Carroll PV. Mechanisms in endocrinology: Hypophysitis: diagnosis and treatment. Eur J Endocrinol. 2018;179(3):R151-R163. doi: https://doi.org/10.1530/EJE-17-0009
4. Gubbi S, Hannah-Shmouni F, Verbalis JG, Koch CA. Hypophysitis: An update on the novel forms, diagnosis and management of disorders of pituitary inflammation. Best Pract Res Clin Endocrinol Metab. 2019;33(6):101371. doi: https://doi.org/10.1016/j.beem.2019.101371
5. Воронцов А.В., Владимирова В.П., Бабаева Д.М. Магнитно-резонансная томография в диагностике эндокринных заболеваний / Под ред. И.И. Дедова. — М.: ООО Медицинское информационное агентство; 2021. 308 с.
6. Kurokawa R, Ota Y, Gonoi W, et al. MRI Findings of Immune Checkpoint Inhibitor-Induced Hypophysitis: Possible Association with Fibrosis. AJNR Am J Neuroradiol. 2020;41(9):1683-1689. doi: https://doi.org/10.3174/ajnr.A6692
7. Naran J, Can AS. Lymphocytic Hypophysitis. [Updated 2020 Nov 29]. In: StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing; [cited 2021 Jan]. Available from: https://www.ncbi.nlm.nih.gov/books/NBK562255/
8. Gutenberg A, Larsen J, Lupi I, et al. A radiologic score to distinguish autoimmune hypophysitis from nonsecreting pituitary adenoma preoperatively. AJNR Am J Neuroradiol. 2009;30(9):1766-1772. doi: https://doi.org/10.3174/ajnr.A1714
9. Prete A, Salvatori R. Hypophysitis. [Updated 2021 Oct 15]. In: Feingold KR, Anawalt B, Boyce A, et al., editors. Endotext [Internet]. South Dartmouth (MA): MDText.com, Inc.; 2000.
10. Bellastella G, Maiorino MI, Bizzarro A, et al. Revisitation of autoimmune hypophysitis: knowledge and uncertainties on pathophysiological and clinical aspects. Pituitary. 2016;19(6):625-642. doi: https://doi.org/10.1007/s11102-016-0736-z
11. Caputo C, Bazargan A, McKelvie PA, et al. Hypophysitis due to IgG4-related disease responding to treatment with azathioprine: an alternative to corticosteroid therapy. Pituitary. 2014;17(3):251-6. doi: https://doi.org/10.1007/s11102-013-0498-9
12. Chiloiro S, Capoluongo ED, Tartaglione T, et al. The Changing Clinical Spectrum of Hypophysitis. Trends Endocrinol Metab. 2019;30(9):590-602. doi: https://doi.org/10.1016/j.tem.2019.06.004
13. Higham CE, Olsson-Brown A, Carroll P, et al. Society for endocrinology endocrine emergency guidance: Acute management of the endocrine complications of checkpoint inhibitor therapy. Endocr Connect. 2018;7(7):G1-G7. doi: https://doi.org/10.1530/EC-18-0068
14. Chiloiro S, Tartaglione T, Capoluongo ED, et al. Hypophysitis Outcome and Factors Predicting Responsiveness to Glucocorticoid Therapy: A Prospective and Double-Arm Study. J Clin Endocrinol Metab. 2018;103(10):3877-3889. doi: https://doi.org/10.1210/jc.2018-01021
15. Wong S, Lam WY, Wong WK, Lee KC. Hypophysitis presented as inflammatory pseudotumor in immunoglobulin G4-related systemic disease. Hum Pathol. 2007 Nov;38(11):1720-3. doi: 10.1016/j.humpath.2007.06.011.
16. Leporati P, Landek-Salgado MA, Lupi I, Chiovato L, Caturegli P. IgG4-related hypophysitis: a new addition to the hypophysitis spectrum. J Clin Endocrinol Metab. 2011 Jul;96(7):1971-80. doi: 10.1210/jc.2010-2970. Epub 2011 May 18.
17. Gubbi S, Hannah-Shmouni F, Verbalis JG, et al. Hypophysitis: An update on the novel forms, diagnosis and management of disorders of pituitary inflammation. Best Pract Res Clin Endocrinol Metab. 2019;33(6):101371. doi: https://doi.org/10.1016/j.beem.2019.101371
18. Ostrov SG, Quencer RM, Hoffman JC, et al. Hemorrhage within pituitary adenomas: how often associated with pituitary apoplexy syndrome? AJR Am J Roentgenol. 1989;153(1):153-160. doi: https://doi.org/10.2214/ajr.153.1.153
19. Faje A. Immunotherapy and hypophysitis: clinical presentation, treatment, and biologic insights. Pituitary. 2016;19(1):82-92. doi: https://doi.org/10.1007/s11102-015-0671-4
20. Faje A. Hypophysitis: Evaluation and Management. Clin Diabetes Endocrinol. 2016;2:15. doi: https://doi.org/10.1186/s40842-016-0034-8
21. Saiwai S, Inoue Y, Ishihara T, et al. Lymphocytic adenohypophysitis: skull radiographs and MRI. Neuroradiology. 1998;40(2):114-120. doi: https://doi.org/10.1007/s002340050550
22. Korkmaz OP, Sahin S, Ozkaya HM, et al. Primary hypophysitis: Experience of a Single Tertiary Center. Exp Clin Endocrinol Diabetes. 2021;129(1):14-21. doi: https://doi.org/10.1055/a-0919-4388
23. Guo S, Wang C, Zhang J, et al. Diagnosis and management of tumor-like hypophysitis: A retrospective case series. Oncol Lett. 2016;11(2):1315-1320. doi: https://doi.org/10.3892/ol.2015.4046
24. Korkmaz OP, Sahin S, Ozkaya HM, et al. Primary hypophysitis: Experience of a Single Tertiary Center. Exp Clin Endocrinol Diabetes. 2021;129(1):14-21. doi: https://doi.org/10.1055/a-0919-4388
25. Joshi MN, Whitelaw BC, Carroll PV. Mechanisms in endocrinology: Hypophysitis: diagnosis and treatment. Eur J Endocrinol. 2018;179(3):R151-R163. doi: https://doi.org/10.1530/EJE-17-0009
26. Honegger J, Buchfelder M, Schlaffer S, et al; Pituitary Working Group of the German Society of Endocrinology. Treatment of Primary Hypophysitis in Germany. J Clin Endocrinol Metab. 2015;100(9):3460-3469. doi: https://doi.org/10.1210/jc.2015-2146
Об авторах
А. В. ВоронцовРоссия
Воронцов Александр Валерьевич, доктор медицинских наук, профессор
117036, Москва, ул. Дм. Ульянова, д. 11
eLibrary SPIN: 2502-4463
Д. М. Бабаева
Бабаева Диана Мажлумовна, врач-рентгенолог
Москва
eLibrary SPIN: 6431-9855;
В. П. Владимирова
Россия
Владимирова Виктория Павловна, кандидат медицинских науr, ведущий научный сотрудник, врач-рентгенолог
Москва
eLibrary SPIN: 9830-3276
Т. А. Дубовицкая
Дубовицкая Татьяна Алексеевна, кандидат медицинских наук, врач-эндокринолог
Москва
eLibrary SPIN: 4380-5447
А. О. Гаврилова
Россия
Гаврилова Алина Олеговна, аспирант
Москва
eLibrary SPIN: 8814-0121
Ж. Е. Белая
Россия
Белая Жанна Евгеньевна, доктор медицинских наук, заведующая отделением нейроэндокринологии и остеопатий
Москва
eLibrary SPIN: 4746-7173
Н. Г. Мокрышева
Россия
Мокрышева Наталья Георгиевна, доктор медицинских наук, профессор, член-корреспондент РАН
Москва
eLibrary SPIN: 5624-3875
Рецензия
Для цитирования:
Воронцов А.В., Бабаева Д.М., Владимирова В.П., Дубовицкая Т.А., Гаврилова А.О., Белая Ж.Е., Мокрышева Н.Г. Клинико-рентгенологическая диагностика гипофизита: обзор литературы и собственные наблюдения. Проблемы Эндокринологии. 2022;68(2):16-33. https://doi.org/10.14341/probl12777
For citation:
Vorontsov A.V., Babaeva D.M., Vladimirova V.P., Dubovitskaya T.A., Gavrilova A.O., Belaya Zh.E., Mokryshevа N.G. Clinical and radiological diagnosis of hypophysitis: a review of literature and own data. Problems of Endocrinology. 2022;68(2):16-33. https://doi.org/10.14341/probl12777
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).








































.jpg)


