Перейти к:
Персонифицированный подход к терапии ожирения на основе доказательных данных и клинических алгоритмов: семаглутид или тирзепатид
https://doi.org/10.14341/probl13677
Аннотация
26 июня 2025 года в Москве прошло заседание экспертной рабочей группы. В центре обсуждения были вопросы персонализированного применения тирзепатида («Тирзетта®») и семаглутида («Велгия ЭКО®») у пациентов с избыточной массой тела, ожирением и сахарным диабетом 2 типа. По итогам встречи была поставлена задача разработать консенсусный алгоритм назначения этих препаратов для их эффективного использования в российской клинической практике.
Для цитирования:
Трошина Е.А., Анциферов М.Б., Аметов А.С., Галстян Г.Р., Маркова Т.Н., Романцова Т.И., Мазурина Н.В., Котешкова О.М. Персонифицированный подход к терапии ожирения на основе доказательных данных и клинических алгоритмов: семаглутид или тирзепатид. Проблемы Эндокринологии. 2025;71(5):19-30. https://doi.org/10.14341/probl13677
For citation:
Troshina E.A., Antsiferov M.B., Ametov A.S., Galstyan G.R., Markova T.N., Romantsova T.I., Mazurina N.V., Koteshkova O.M. A personalized, evidence-based approach to obesity therapy using clinical algorithms: semaglutide or tirzepatide. Problems of Endocrinology. 2025;71(5):19-30. (In Russ.) https://doi.org/10.14341/probl13677
Эпидемическое распространение ожирения и сахарного диабета 2 типа (СД2), ассоциированных с высоким кардиометаболическим риском, представляет собой одну из наиболее серьезных угроз общественному здоровью в XXI веке. Традиционные терапевтические подходы демонстрируют ограниченную эффективность в отношении снижения массы тела и сердечно-сосудистых исходов в долгосрочной перспективе. Появление и внедрение в клиническую практику препаратов на основе механизма действия инкретинов ознаменовало новую эру в лечении метаболических заболеваний. Агонисты рецепторов глюкагоноподобного пептида-1 (арГПП-1) и, впоследствии двойные и мультиагонисты, оказывают комплексное воздействие на ключевые патофизиологические звенья СД2 и ожирения. Эти препараты не только эффективно контролируют уровень глюкозы и массу тела, но и демонстрируют плейотропные эффекты в отношении сердечно-сосудистой системы, неалкогольной жировой болезни печени (НАЖБП), хронической болезни почек (ХБП), синдрома обструктивного апноэ сна (СОАС) и остеоартрита (ОСА), что делает их важнейшей составляющей современной персонализированной терапии [1][2].
26 июня 2025 г. в Москве состоялось совещание рабочей группы экспертов на тему «Обсуждение персонификации терапии тирзепатидом (Тирзетта) и семаглутидом (Велгия ЭКО) и подготовка алгоритма их назначения пациентам с избыточным весом или ожирением, в том числе с СД 2 типа». Целью совещания была выработка консенсусной позиции по оптимальному применению агонистов инкретиновых рецепторов в реальной клинической практике с учетом актуальных международных и отечественных данных. История создания этих препаратов началась с изучения редкой ядовитой ящерицы Gila Monster (Heloderma suspectum). Это животное, обитающее в пустынях Аризоны вблизи реки Gila, проводит до 90% времени под землей и питается очень редко, что натолкнуло ученых на мысль об уникальных механизмах регуляции метаболизма [3][4]. В слюне этой ящерицы был обнаружен пептид эксендин-4, ставший прототипом для разработки первого агониста рецепторов ГПП-1 [5]. Как было отмечено в одном из выпусков журнала “Diabetologia”, препараты на основе эффектов инкретинов стали своего рода антидотом для множества заболеваний, связанных с диабетом и ожирением [6].
Несмотря на то, что оба препарата относятся к одному классу, их молекулярные механизмы и, как следствие клинические эффекты, имеют существенные различия. Семаглутид — агонист единственного рецептора, глюкагоноподобного пептида-1 (ГПП-1), с периодом полувыведения около недели (160 часов). Тирзепатид — это двойной агонист, воздействующий как на рецепторы ГПП-1, так и на рецепторы глюкозозависимого инсулинотропного полипептида (ГИП). Период полувыведения тирзепатида несколько короче — порядка 5 дней (116,7 часа). Аффинность тирзепатида к рецептору ГИП сопоставима с аффинностью нативного гормона, аффинность к рецептору ГПП-1 в 5 раз слабее. Рецепторы инкретинов относятся к классическим рецепторам, сопряженным с G-белками [7][8]. Рецепторы содержат большой внеклеточный N-концевой домен, отвечающий за связывание лиганда, 7 трансмембранных α-спиралей и внутриклеточный С-концевой домен, который взаимодействует с G-белками и другими сигнальными молекулами. При связывании с лигандом рецептор претерпевает конформационные изменения, которые активируют внутриклеточные сигнальные каскады за счет сопряжения со стимулирующим G-белком, что приводит к активации аденилатциклазы и последующему повышению уровня циклического аденозинмонофосфата (цАМФ), что в итоге приводит к соответствующему клеточному ответу (повышению секреции инсулина в β-клетках, высвобождению нейротрансмиттеров в нейронах и т.д.). Помимо повышения ПКА, взаимодействие рецепторов с лигандом сопровождается рекрутированием β-аррестина, который способствует интернализации рецепторов, уменьшению их количества на клеточной мембране. Вместе с фрагментом мембраны рецептор погружается в цитоплазму клетки, формируя эндосомальный компартмент. Некоторые эндосомальные компартменты вновь возвращаются к мембране, в то время как другие сливаются с лизосомами. Семаглутид является сбалансированным лигандом по отношению к рецепторам ГПП-1. Его взаимодействие с рецепторами сопровождается как повышением ПКА, так и рекрутированием β-аррестина. Тирзепатид — сбалансированный лиганд по отношению к рецепторам ГИП, но смещенный лиганд по отношению к рецепторам ГПП-1: активация внутриклеточных сигнальных путей сопровождается минимальным рекрутированием β-аррестина и, соответственно, снижением десенситизации рецепторов ГПП-1. Эти особенности фармакодинамики во многом объясняют более выраженное влияние тирзепатида на массу тела и углеводный обмен по сравнению с арГПП-1 [9][10].
Рецепторы инкретинов расположены на всех трех основных типах островковых типах клеток: альфа, бета, дельта. Оба препарата усиливают секрецию инсулина и соматостатина, подавляют апоптоз бета-клеток поджелудочной железы. Семаглутид подавляет секрецию глюкагона. Тирзепатид в изолированных островковых клетках увеличивает секрецию глюкагона. У больных СД2 на фоне лечения препаратом происходит постепенное снижение содержания гормона [11][12][13].
ВЛИЯНИЕ НА ЦЕНТРАЛЬНУЮ НЕРВНУЮ СИСТЕМУ И КОНТРОЛЬ АППЕТИТА
Рецепторы инкретинов расположены в ключевых зонах мозга, отвечающих за контроль аппетита и пищевого поведения, включая гипоталамус, ствол мозга и систему вознаграждения, что объясняет их комплексное анорексигенное действие. Семаглутид воздействует на более обширные зоны мозга, чем его предшественники. Кроме того, препарат повышает продукцию пролактин- релизинг-гормона (мощного анорексигенного нейромедиатора) и тирозингидроксилазы, участвующей в синтезе дофамина [14]. Тирзепатид реализует более выраженный эффект подавления аппетита путем активации обоих видов инкретиновых рецепторов на уровне гипоталамуса и ствола мозга, а также способствуя повышению проницаемости гематоэнцефалического барьера для периферических анорексигенных гормонов [15][16]. Оба препарата снижают тягу к сладкой, жирной и соленой пище и показывают положительные результаты в лечении различных форм зависимостей, в том числе алкогольной [17].
ПЕРЕНОСИМОСТЬ: ПОЧЕМУ ТИРЗЕПАТИД В МЕНЬШЕЙ СТЕПЕНИ ВЫЗЫВАЕТ ТОШНОТУ?
Одним из главных преимуществ тирзепатида является его лучшая переносимость в отношении возникновения тошноты и рвоты. Механизм этого обусловлен двойном действием на «рвотный центр» в стволе мозга (area postrema).
Нейроны, экспрессирующие рецепторы обоих инкретинов, относительно малочисленны. В большинстве случаев рецепторы ГИП и ГПП-1 локализованы в различных популяциях нейронов. Эти анатомические особенности свидетельствуют о том, что агонисты ГПП-1р и ГИПр влияют на разные нейронные цепи [18]. В области area postrema подавляющее большинство нейронов, экспрессирующих рецепторы ГИП — ГАМКергические (ингибирующие), а большинство ГПП-1р-содержащих нейронов — глутаматергические (возбуждающие). Активация рецепторов ГПП-1 (как в случае семаглутида) возбуждает эти нейроны, вызывая не только снижение аппетита, но и тошноту. Под действием тирзепатида активация нейронов, экспрессирующих рецепторы ГИП на уровне area postrema, сопровождается выработкой гамма-амино-масляной кислоты (ГАМК), что подавляет активность нейронов, содержащих рецепторы ГПП-1, тем самым значительно снижая риск развития тошноты и рвоты [19]. Кроме того, тирзепатид подавляет эффекты пептида YY на уровне area postrema (попытки разработать моноагонисты рецепторов пептида YY для фармакотерапии ожирения не увенчались успехом вследствие выраженной тошноты и рвоты на фоне их применения) [20].
ЖЕЛУДОЧНО-КИШЕЧНЫЙ ТРАКТ И ЛЕКАРСТВЕННЫЕ ВЗАИМОДЕЙСТВИЯ
Степень замедления моторики желудка у тирзепатида и семаглутида сопоставимы (исследования проведены у животных, у пациентов с СД2, с ожирением) [21]. Замедление опорожнения желудка на фоне обоих препаратов относится к числу их периферических механизмов снижения массы тела. Однако этот эффект требует внимания при выполнении эндоскопии либо оперативных вмешательств вследствие повышения риска регургитации и легочной аспирации. Анестезиологи рекомендуют отменять препараты минимум за 1 неделю до планируемых вмешательств, однако этот период может оказаться недостаточным для полного восстановления функции желудка. Оптимальная продолжительность прекращения приема GLP-1RA для снижения риска аспирации в настоящее время неизвестна, тщательные исследования в этой области продолжаются [22]. Изменение моторной функции желудочно-кишечного тракта может влиять на фармакокинетику других применяемых пациентом препаратов. Клинически значимое снижение абсорбции пероральных контрацептивов подтверждено на фоне применения тирзепатида, L-тироксина — на фоне терапии семаглутидом [23].
ВОСПАЛЕНИЕ И ЖИРОВАЯ ТКАНЬ
Хроническое воспаление — ключевой фактор развития осложнений ожирения. Как семаглутид, так и тирзепатид, эффективно подавляют воспаление. Механизмы, посредством которых препараты влияют на воспалительные процессы, имеют существенные отличия. Рецепторы ГПП-1 на клетках иммунной системы экспрессированы достаточно скудно. Семаглутид непосредственно снижает локальное воспаление лишь в ЖКТ путем активации Т-лимфоцитов. Системное воспаление на фоне семаглутида снижается путем активации центральных рецепторов ГПП-1 с участием адренергических и опиоидных рецепторов. Тирзепатид действует напрямую на иммунные клетки, которые несут на своей поверхности большое количество рецепторов ГИП [24].
В жировой ткани рецепторы ГПП-1 до настоящего времени не идентифицированы. Преимущественно посредством вовлечения симпатической нервной системы в белой жировой ткани семаглутид снижает воспаление, активирует липолиз, захват липидов, снижает содержание висцерального эктопического жира, повышает конверсию белых адипоцитов в бежевые и термогенез [25]. Рецепторы ГИП экспрессируются на многих клетках жировой ткани, включая бурые и бежевые адипоциты, макрофаги, перициты, мезотелий [12][26]. Тирзепатид оказывает прямое влияние на жировую ткань. Активация рецепторов ГИП под действием тирзепатида в белой жировой ткани способствует повышению кровотока (транспорт нутриентов и кислорода), чувствительности адипоцитов к инсулину, захвата глюкозы и СЖК, липогенезу de novo. Повышение термогенеза под действием тирзепатида реализуется на основе не только классических механизмов (повышение экспрессии белка UCP-1, разобщающего окислительное фосфорилирование), но и путем UCP-1-независимого футильного кальциевого цикла [27].
ЗАЩИТА ОРГАНОВ-МИШЕНЕЙ
Сердце и сосуды. Препараты обладают мощным кардиопротективным действием, снижая воспаление, улучшая сократимость миокарда и стабилизируя атеросклеротические бляшки. Семаглутид одобрен для снижения сердечно-сосудистых рисков [28].
Почки. Семаглутид снижает риск прогрессирования хронической болезни почек у пациентов с СД и одобрен для применения в этой группе пациентов. Тирзепатид также демонстрирует впечатляющие результаты в этой области [29].
Мозг. Оба препарата оказывают нейропротективное действие, снижая нейровоспаление и накопление амилоида, что открывает перспективы для лечения нейродегенеративных заболеваний [30].
Легкие. Тирзепатид рекомендован для лечения синдрома обструктивного апноэ сна, что является большим преимуществом для пациентов с ожирением [31].
Глубокое понимание уникальных механизмов действия семаглутида и тирзепатида является ключом к максимально эффективному и безопасному применению этих инновационных препаратов в клинической практике. В свою очередь, анализ данных имеющихся рандомизированных клинических исследований (РКИ) позволяет сформировать практические подходы к выбору терапии: от общих установок к персонализированной, доказательной медицине.
ОТ КИЛОГРАММОВ К КЛИНИЧЕСКИМ ИСХОДАМ: ПОСТАНОВКА ЦЕЛЕЙ ТЕРАПИИ
В лечении ожирения крайне важно определять индивидуальные цели для каждого пациента, выходя за рамки простого снижения веса. Была предложена четкая градация терапевтических целей (табл. 1):
- снижение веса на 5–10%: уменьшение симптоматики и улучшение качества жизни;
- снижение веса более чем на 15%: такой результат необходим для достижения более амбициозных целей, таких как ремиссия сопутствующих заболеваний, снижение смертности и предотвращение тяжелых осложнений, включая сердечную недостаточность и другие сердечно-сосудистые события [32].
Таблица 1. Улучшение течения сопутствующих состояний зависит от процента снижения массы тела

ПРЯМОЕ СРАВНЕНИЕ ТИРЗЕПАТИДА И СЕМАГЛУТИДА В ИССЛЕДОВАНИИ SURMOUNT-5
Ключевым для понимания эффективности стало исследование SURMOUNT-5, в котором напрямую сравнивались максимальные дозы тирзепатида (15 мг) и семаглутида (2,4 мг) у пациентов с ожирением, но без СД. Продолжительность исследования составила 72 недели (табл. 2).
Таблица 2. Surmount-5: ожирение и избыточная масса тела
Цель терапии: профилактика развития осложнений
Показатель эффективности: % снижения массы тела, ↓окружности талии
|
Параметр |
Семаглутид 2,4 мг |
Тирзепатид 15 мг |
|
Средняя потеря веса |
-13,7% (95% ДИ: -14,9 до -12,6) |
-20,2% (95% ДИ: -21,4 до -19,1) |
|
Абсолютная потеря веса |
-15,0 кг (95% ДИ: -16,3 до -13,7) |
-22,8 кг (95% ДИ: -24,1 до -21,5) |
|
Уменьшение окружности талии |
-13,0 см (95% ДИ: -14,3 до -11,7) |
-18,4 см (95% ДИ: -19,6 до -17,2) |
|
Снижение ИМТ |
-6,0 кг/м² |
-8,5 кг/м² |
|
Достижение целевых показателей потери веса |
||
|
≥10% |
60,5% |
81,6% |
|
≥15% |
40,1% |
64,6% |
|
≥20% |
27,3% |
48,4% |
|
≥25% |
16,1% |
31,6% |
|
≥30% |
6,9% |
19,7% |
Значения представлены в виде расчетной разницы в процентных пунктах между группами, за исключением категорий снижения веса, которые составляют не менее 10%, 15%, 20%, 25%, и 30%, которые указаны как относительный риск. Относительный риск был рассчитан с использованием G-методы расчета на основе логистической регрессии.
P<0,001 для всех первичных и ключевых вторичных конечных точек.
Эффективность: тирзепатид продемонстрировал статистически значимое преимущество по всем ключевым показателям снижения веса, включая среднюю и абсолютную потерю массы тела, а также уменьшение окружности талии. Так, 81% пациентов на тирзепатиде и 60% на семаглутиде достигли снижения веса на 10% и более, что является клинически значимым результатом для прогноза.
Безопасность и переносимость: общая частота нежелательных явлений была сопоставимой между двумя препаратами. Наиболее частыми побочными эффектами со стороны ЖКТ были тошнота (около 44% в обеих группах), запор (28%) и диарея (23%). Важно отметить, что частота серьезных нежелательных явлений, приведших к прекращению терапии (включая панкреатит и сердечно-сосудистые события), была очень низкой и не различалась между группами [33].
ВЛИЯНИЕ НА СОПУТСТВУЮЩИЕ ЗАБОЛЕВАНИЯ: ДАННЫЕ КЛИНИЧЕСКИХ ИССЛЕДОВАНИЙ
Сердечно-сосудистые риски
Семаглутид. Исследование SELECT стало прорывным, доказав, что препарат в дозе 2,4 мг снижает риск серьезных сердечно-сосудистых событий (MACE) на 20% у пациентов с ожирением и установленными ССЗ, но без СД (табл. 3). Эффект наблюдался практически с самого начала терапии, что указывает на прямые кардиопротективные механизмы, а не только как на результат снижения веса [34]. Данные реальной практики, полученные в исследования SCORE, оказались еще более впечатляющими, показав снижение общей смертности на 86% [35]. Эти результаты позволили зарегистрировать новое показание для семаглутида — снижение риска сердечно-сосудистых событий у пациентов с ожирением.
Таблица 3. Семаглутид/Тирзепатид: влияние на течение АССЗ
Цель терапии: снижение рисков сердечно-сосудистых катастроф
|
Параметр |
Семаглутид 2,4 мг (SELECT) |
Тирзепатид 15 мг (SURMOUNT-MMO) |
|
MACE |
-20% P<0,001 for superiority |
В процессе изучения |
|
Смерть от всех причин |
-19% |
|
|
Нефатальный инфаркт миокарда |
-28% |
|
|
СС смертность |
-15% P=0,07 |
|
|
Развитие и усугубление ХБП |
-22% |
|
|
Развитие и усугубление ХСН |
-18% |
Тирзепатид. Аналогичное исследование SURMOUNT-MMO для препарата еще продолжается. Ожидается, что его результаты также будут положительными.
ВЛИЯНИЕ НА ХРОНИЧЕСКУЮ СЕРДЕЧНУЮ НЕДОСТАТОЧНОСТЬ С СОХРАННОЙ ФРАКЦИЕЙ ВЫБРОСА (ХСННФВ)
Тирзепатид 15 мг. В исследовании SUMMIT препарат продемонстрировал выраженный эффект, снизив риск госпитализаций по поводу ХСН на 38% [36].
Семаглутид 2,4 мг. Показано значительное улучшение показателей по шкалам оценки качества жизни и тестам с шестиминутной ходьбой, а также снижение уровня С-реактивного белка [37]. В исследовании реальной практики SCORE снижение риска СН достигло 54% (табл. 4) [35].
Таблица 4. Семаглутид/Тирзепатид: влияние лечения на ХСНСФВ у пациентов с ожирением
Цель терапии: ↓числа госпитализаций, улучшение функциональной активности больных
|
Параметр |
Семаглутид 2,4 мг (STEP-HFpEF) |
Тирзепатид 15 мг (SUMMIT) |
|
Продолжительность исследования |
52 недели |
104 недели |
|
Снижение риска госпитализаций и ухудшения ХСН |
STEP-HFpEF не оценивали в рамках КИ; SCORE (120 недель): -54% HR 0,46 (95% ДИ: 0,29–0,73, p<0,05) |
-38% HR 0,62 (95% ДИ: 0,41–0,95; p=0,026) |
|
Улучшение KCCQ-CSS |
+7,8 баллов (p<0,001) |
+6,9 баллов (p<0,001) |
|
Улучшение 6-мин теста |
+21,5 м (разница: +20,3 м; p<0,001) |
+26,0 м (разница: +18,3 м; p<0,001) |
|
Снижение вчСрб |
-43,5% (разница: -36,2%, p<0,001) |
-38,8% (разница: -34,9%) |
СИНДРОМ ОБСТРУКТИВНОГО АПНОЭ СНА (СОАС)
Тирзепатид является единственным препаратом, у которого есть завершенное РКИ и официальное одобрение для лечения СОАС средней и тяжелой степени тяжести у взрослых с ожирением в сочетании с низкокалорийной диетой и повышенной физической активностью. Исследование показало значительное снижение количества приступов апноэ/гипопноэ в час (табл. 5) [38].
Таблица 5. Семаглутид/Тирзепатид: влияние лечения на течение синдрома обструктивного апноэ сна у пациентов с ожирением
Цель терапии: изменение индекса апноэ–гипопноэ (AHI, количество приступов апноэ и гипопноэ в течение часа сна) по сравнению с исходным уровнем
|
Параметр |
Семаглутид 2,4 мг |
Тирзепатид 15 мг (SURMOUNT-OSA) |
|
Характеристика пациентов |
Не изучался |
ИМТ: не менее 30 кг/м² (в среднем 39 кг/м²) Индекс апноэ-гипопноэ: не менее 15 событий за час (в среднем 50) Пациенты без СД1 и СД2 |
|
Изменение индекса апноэ–гипопноэ |
-29 эпизодов 95% ДИ, −33,2 to −25,4, P<0,001 |
ОСТЕОАРТРИТ КОЛЕННОГО СУСТАВА
Семаглутид имеет доказательную базу по положительному влиянию на остеоартрит, что связано не только со снижением нагрузки на суставы, но и с прямым противовоспалительным действием. В ходе клинического исследования STEP-9 продемонстрировано значимое снижение болевого синдрома и улучшение функциональной активности по шкале WOMAC у пациентов с ожирением и остеоартритом коленного сустава (табл. 6) [39].
Таблица 6. Семаглутид/Тирзепатид: влияние лечения на течение остеоартрита коленного сустава
Цель терапии: снижение болевого синдрома, улучшение функциональной подвижности
|
Параметр |
Семаглутид 2,4 мг (STEP-9) |
Тирзепатид 15 мг |
|
Характеристика пациентов |
407 пациентов, возраст 56 лет, ИМТ 40,3, ср. значение по шкале боли WOMAC 70,9 |
Не изучался |
|
Снижение болевого синдрома по шкале WOMAC |
-41,7 |
|
|
Улучшение функциональной подвижности за счет снижения скованности по шкале WOMAC |
-41,5 |
НЕАЛКОГОЛЬНАЯ/МЕТАБОЛИЧЕСКИ АССОЦИИРОВАННАЯ ЖИРОВАЯ БОЛЕЗНЬ ПЕЧЕНИ (НАЖБП/МАЖБП)
Исследование 2 фазы SYNERGY-NASH продемонстрировало потенциальный положительный эффект при применении тирзепатида 15 мг и способствовало разрешению стеатогепатита у 62% пациентов и уменьшению стадии фиброза у 51% из них. На сегодняшний день данный препарат изучается в клинических испытаниях 3-й фазы [40] (табл. 7).
Таблица 7. Семаглутид/Тирзепатид: влияние на развитие и течение НАЖБП
Цель терапии: разрешение стеатогепатоза и уменьшение стадии фиброза
|
Параметр |
Семаглутид 2,4 мг (ESSENCE 3 фаза, промежуточные результаты) |
Тирзепатид (SYNERGY-NASH 2 фаза) |
|
Разрешение стеатогепатоза без ухудшения степени фиброза печени |
62,9% |
62% |
|
Уменьшение стадии фиброза, без прогрессирования стеатогепатоза |
37% |
51% |
Применение Семаглутида 2,4 мг в исследовании ESSENCE способствовало разрешению стеатогепатита у 62,9% пациентов и уменьшению стадии фиброза у 37% [41]. В 2025 г. FDA одобрило применение семаглутида для лечения метаболически ассоциированного стеатогепатита (MASH), также известного как неалкогольная жировая болезнь печени, у взрослых с фиброзом средней и высокой степени выраженности.
ПРЕДИАБЕТ / ПРОФИЛАКТИКА СД2
Семаглутид 2,4 мг и тирзепатид 15 мг продемонстрировали нормализацию гликемии у 81% и 95% пациентов соответственно, что свидетельствует об эффективной профилактике развития СД2 у пациентов с ожирением и предиабетом (табл. 8) [42][ 43].
Таблица 8. Семаглутид/Тирзепатид: влияние на риск развития сахарного диабета 2 типа у больных с ожирением и предиабетом
Цель терапии: нормализация уровня гликемии, снижение массы тела
|
Параметр |
Семаглутид 2,4 мг (STEP-10) |
Тирзепатид 15 мг (SURMOUNT-1) |
|
Характеристика пациентов |
207 участников, возраст 53±11 лет, ИМТ 40,1±6,9 кг/м², HbA1c 5,9%±0,3 |
1032 участников, возраст 48,2±11,8, ИМТ 38,8±7,10 кг/м², НbA1c 5,8 ± 0,34 % |
|
Изменение массы тела от исх. |
-14% |
-23% |
|
Нормализация гликемии, % пациентов |
81% |
95% |
САХАРНЫЙ ДИАБЕТ 2 ТИПА У ПАЦИЕНТОВ С ОЖИРЕНИЕМ
Оба препарата эффективны для контроля гликемии и снижения веса у пациентов с СД2 и сопутствующим ожирением (табл. 9). Тирзепатид 15 мг показал более выраженное снижение гликированного гемоглобина (HbA1c) (–2,08% vs –1,6%) и большую долю пациентов, достигших целевых значений. Однако следует отметить, что увеличение дозы семаглутида с 1,0 мг до 2,4 мг также способствует выраженному снижению массы тела и контролю гликемии у данной группы пациентов [44][ 45].
Таблица 9. Семаглутид/Тирзепатид: влияние на показатели углеводного обмена у больных с сахарным диабетом 2 типа и ожирением
Цель терапии: нормализация уровня гликемии, снижение массы тела
|
Параметр |
Семаглутид (STEP 2) |
Тирзепатид (SURMOUNT-2) |
|
Снижение HbA1c |
–1,6% |
–2,08% |
|
Доля пациентов с HbA1c <7% |
78,5% |
84% |
|
Доля с нормогликемией (HbA1c <6,5%) |
67,5% |
79% |
|
Доля с нормогликемией (HbA1c <5,7%) |
Не сообщается |
49% |
|
Гипогликемия |
5,7% пациентов |
5% пациентов |
|
Тяжелая гипогликемия |
1 случай |
0 случаев |
В арсенале российских врачей появились 2 препарата, которые обеспечивают выраженное снижение массы тела и контроль коморбидных состояний. В связи с этим возникает вопрос персонификации их выбора для лечения пациентов с ожирением и избыточной массой тела, оценки эффективности проводимых мероприятий. Решение этих непростых задач и легло в основу научной дискуссии экспертов, включая:
1) определение групп пациентов с ожирением для персонифицированного назначения тирзепатида /семаглутида 2,4 мг;
2) выбор терапии тирзепатидом /семаглутидом 2,4 мг с учетом профилактики сердечно-сосудистых осложнений;
3) алгоритм перевода с семаглутида на тирзепатид.
ВОПРОС 1: ОПРЕДЕЛЕНИЕ ГРУПП ПАЦИЕНТОВ С ОЖИРЕНИЕМ ДЛЯ ПЕРСОНИФИЦИРОВАННОГО НАЗНАЧЕНИЯ ТИРЗЕПАТИДА / СЕМАГЛУТИДА 2,4 МГ
Выбор семаглутида или тирзепатида должен основываться на оценке следующих ключевых параметров (рис. 1, 2):
- исходных антропометрических показателей,
- целей по снижению массы тела,
- предыдущего опыта терапии,
- структуры коморбидности.

Рисунок 1. Параметры, влияющие на выбор стартового препарата.
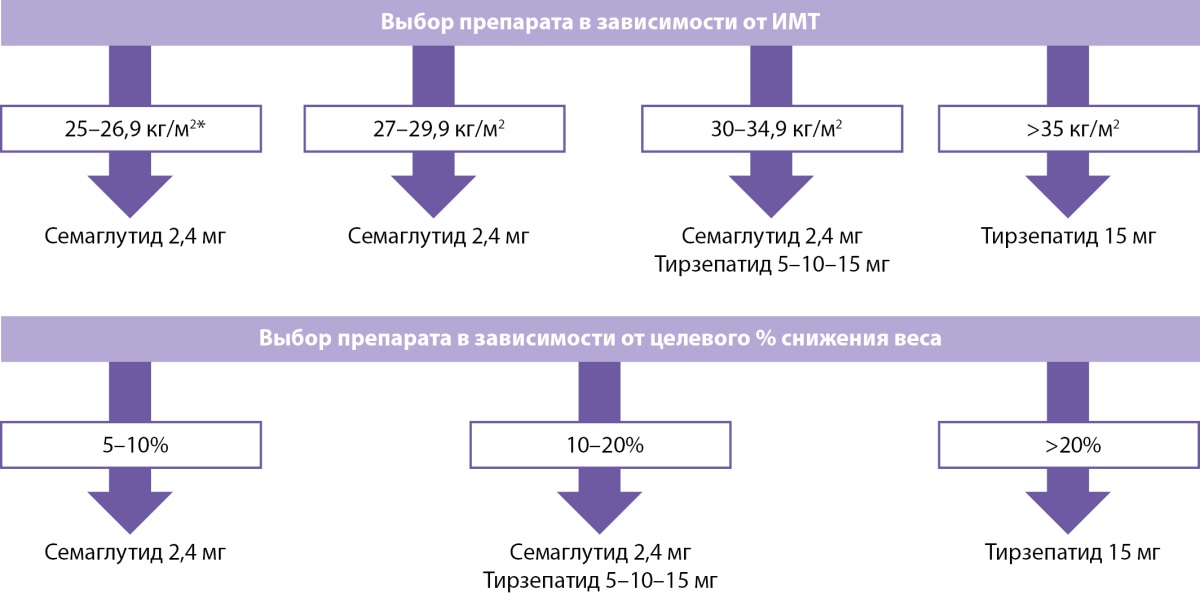
Рисунок 2. Исходные антропометрические параметры
Примечание: *ИМТ 25–27 кг/м² при наличии осложнений, таких как АГ, дислипидемия, НАЖБП, СОАС, предиабет и СД2 — согласно клиническим рекомендациям ожирение 1 стадия.
ИМТ 27–29,9 кг/м² (при наличии сопутствующих заболеваний: АГ, дислипидемия, НАЖБП, СОАС, предиабет, СД2): стартовая терапия — семаглутид 2,4 мг.
- ИМТ 30—34,9 кг/м²: семаглутид 2,4 мг или тирзепатид 5–10–15 мг.
- ИМТ ≥35 кг/м²: предпочтительная терапия — тирзепатид 15 мг.
Цели по снижению массы тела:
- целевое снижение массы тела 5–20%: семаглутид 2,4 мг или тирзепатид 5–10–15 мг.
- целевое снижение массы тела >20%: предпочтительная терапия — тирзепатид 15 мг.
Предыдущий опыт терапии и переносимость семаглутида (рис. 3):
- положительный опыт применения семаглутида: титрация и использование терапевтической дозы 2,4 мг;
- положительный опыт применения семаглутида, но недостижение целей на дозе 1,0 мг (off-label или при СД2): переход на семаглутид 2,4 мг;
- неудовлетворительная переносимость на любых дозах семаглутида: переход на тирзепатид 2,5 мг;
- недостижение целей по снижению веса на фоне хорошей переносимости семаглутида 2,4 мг — переход на тирзепатид 5 мг для интенсификации терапии.
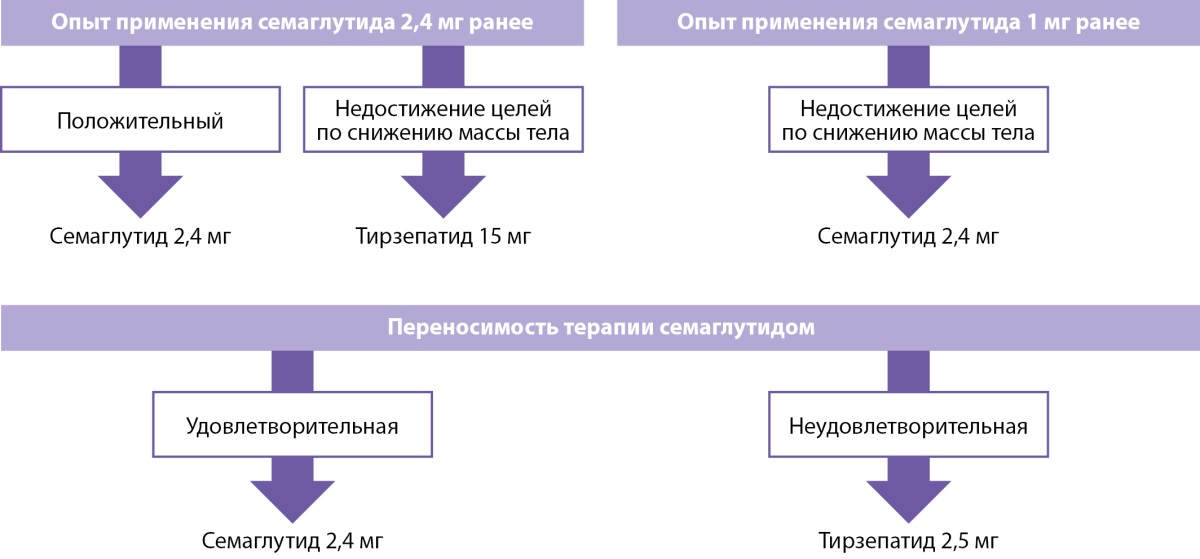
Рисунок 3. Выбор препарата для лечения ожирения в зависимости от предыдущего опыта применения или переносимости семаглутида.
Оценка эффективности терапии рекомендуется через 3 месяца после достижения максимальной терапевтической дозы (2,4 мг для семаглутида, 15 мг для тирзепатида). Минимальная рекомендуемая длительность терапии при хорошей переносимости составляет не менее 2 лет.
Выбор терапии с учетом коморбидных состояний
Наличие специфических коморбидных состояний определяет предпочтение в выборе препарата с наибольшей доказательной базой для конкретной патологии (рис. 4):

Рисунок 4. Выбор препарата для лечения ожирения в зависимости от коморбидных состояний.
Следует отметить, что несмотря на доказанные преимущества тирзепатида у пациентов с СД2, увеличение дозы семаглутида с 1,0 мг до 2,4 мг может являться приоритетной рекомендацией, учитываю его статус списке ЖНВЛП и доступность.
ВОПРОС 2: ВЫБОР ТЕРАПИИ ТИРЗЕПАТИДОМ/СЕМАГЛУТИДОМ С УЧЕТОМ ПРОФИЛАКТИКИ СЕРДЕЧНО-СОСУДИСТЫХ ОСЛОЖНЕНИЙ
Назначение семаглутида 2,4 мг является приоритетной рекомендацией у пациентов с ожирением и сердечно-сосудистыми заболеваниями (ССЗ), поскольку он является единственным препаратом для лечения ожирения, обладающим официально зарегистрированным показанием для снижения риска основных неблагоприятных сердечно-сосудистых событий (MACE), что доказано результатами масштабного исследования SELECT: на фоне терапии было зафиксировано достоверное снижение риска MACE на 20%, сердечно-сосудистой смертности на 15% и смерти от всех причин на 19%.
ВОПРОС 3: АЛГОРИТМ ПЕРЕВОДА С СЕМАГЛУТИДА НА ТИРЗЕПАТИД
Перевод пациента с одного препарата на другой должен осуществляться в рамках подхода «шаг за шагом» (рис. 5).
- Для интенсификации терапии при недостижении целей по снижению веса на фоне хорошей переносимости семаглутида 2,4 мг рекомендуется переход на тирзепатид в стартовой дозе 5 мг с последующей титрацией до 15 мг.
- При непереносимости семаглутида на любом этапе титрации (дозы 0,25–2,4 мг) рекомендуется переход на тирзепатид в стартовой дозе 2,5 мг с последующей титрацией до 15 м.
- У пациентов с СД2, получающих семаглутид 1,0 мг:
- для интенсификации сахароснижающей терапии и дальнейшего снижения веса возможен переход на семаглутид 2,4 мг;
- при недостижении целей по контролю гликемии возможен переход на тирзепатид 5 мг (данные исследования SURPASS-SWITCH-2);
- при непереносимости — переход на тирзепатид 2,5 мг.
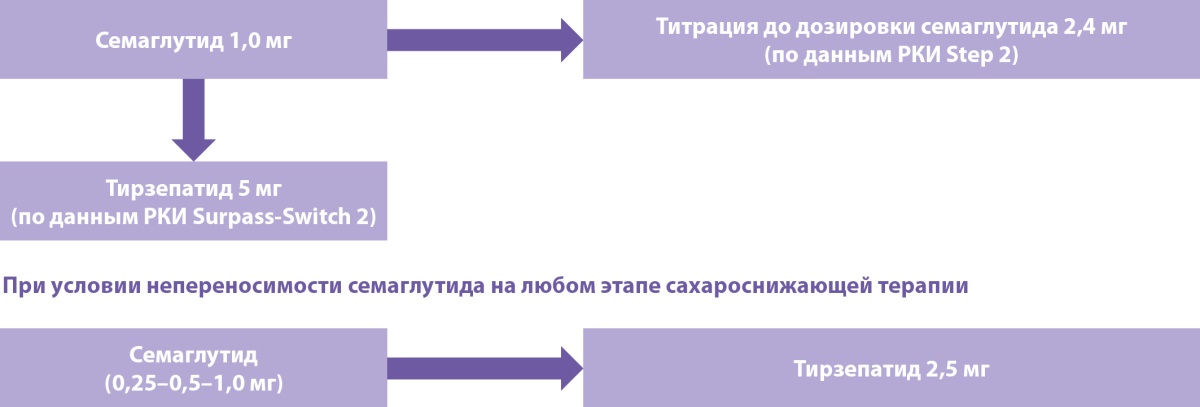
Рисунок 5. Алгоритм перехода с семаглутида 2,4 мг на тирзепатид у пациентов с ожирением + СД2.
МОНИТОРИНГ ЭФФЕКТИВНОСТИ И БЕЗОПАСНОСТИ
Оценка эффективности терапии должна быть комплексной и включать:
- динамику массы тела и антропометрических показателей (окружность талии и бедер, ИМТ);
- достижение целевых показателей (% снижения массы тела, целевые значения HbA1cпри СД2);
- влияние на коморбидные состояния (контроль АД, липидный спектр, показатели функции печени, индекс апноэ-гипопноэ при СОАС, оценка по шкалам боли и качества жизни);
- оценку переносимости, особенно со стороны ЖКТ (тошнота, рвота, диарея, запор).
ЗАКЛЮЧЕНИЕ
- Семаглутид 2,4 мг (Велгия ЭКО®) и тирзепатид (Тирзетта®) являются высокоэффективными препаратами для лечения ожирения и управления метаболическим здоровьем. Выбор между ними должен быть персонифицированным.
- При наличии НАЖБП, заболеваний суставов или АССЗ для снижения риска MACE предпочтение следует отдавать семаглутиду 2,4 мг.
- Для достижения максимального снижения массы тела (>20%), при наличии ожирение 2–3 ст. (ИМТ≥35 кг/м²) или СОАС предпочтительным выбором является назначение тирзепатида 15 мг.
- Предложен алгоритм перевода с семаглутида на тирзепатид для интенсификации терапии или в случае непереносимости.
- Рекомендуется внедрить предлагаемые алгоритмы выбора в клиническую практику эндокринологов, врачей общей практики, терапевтов, кардиологов и др.
ДОПОЛНИТЕЛЬНАЯ ИНФОРМАЦИЯ
Источники финансирования. Работа выполнена по инициативе авторов без привлечения финансирования.
Конфликт интересов. Авторы декларируют отсутствие явных и потенциальных конфликтов интересов, связанных с содержанием настоящей статьи.
Участие авторов. Все авторы одобрили финальную версию статьи перед публикацией, выразили согласие нести ответственность за все аспекты работы, подразумевающую надлежащее изучение и решение вопросов, связанных с точностью или добросовестностью любой части работы.
Список литературы
1. McGowan B, Ciudin A, Baker JL, et al. Framework for the pharmacological treatment of obesity and its complications from the European Association for the Study of Obesity (EASO). Nat Med. 2025. doi: https://doi.org/10.1038/s41591-025-03765-w
2. Nauck MA, Quast DR, Wefers J, Pfeiffer AFH. The evolving story of incretins (GIP and GLP-1) in metabolic and cardiovascular disease: A pathophysiological update. Diabetes Obes Metab. 2021;23 Suppl 3:5-29. doi: https://doi.org/10.1111/dom.14496
3. Christel CM, DeNardo DF, Secor SM. Metabolic and digestive response to food ingestion in a binge-feeding lizard, the Gila monster (Heloderma suspectum). J Exp Biol. 2007;210(Pt 19):3430-9. doi: https://doi.org/10.1242/jeb.004820
4. Park JS, Kim KS, Choi HJ. Glucagon-Like Peptide-1 and Hypothalamic Regulation of Satiation: Cognitive and Neural Insights from Human and Animal Studies. Diabetes Metab J. 2025;49(3):333-347. doi: https://doi.org/10.4093/dmj.2025.0106
5. Eng J, Kleinman WA, Singh L, et al. Isolation and characterization of exendin-4, an exendin-3 analogue, from Heloderma suspectum venom. Further evidence for an exendin receptor on dispersed acini from guinea pig pancreas. J Biol Chem. 1992;267(11):7402-5
6. Krook A, Mulder H. Incretins: turning the venom into the antidote. Diabetologia. 2023;66(10):1762-1764. doi: https://doi.org/10.1007/s00125-023-05987-4
7. De Graaf C, Donnelly D, Wootten D, et al. Glucagon-Like Peptide-1 and Its Class B G Protein-Coupled Receptors: A Long March to Therapeutic Successes. Pharmacol. Rev. 2016;68:954–1013. doi: https://doi.org/10.1124/pr.115.011395
8. Coskun T, Sloop KW, Loghin C, et al. LY3298176, a novel dual GIP and GLP-1 receptor agonist for the treatment of type 2 diabetes mellitus: From discovery to clinical proof of concept. Mol Metab. 2018; 18:3-14. doi: https://doi.org/10.1016/j.molmet.2018.09.009
9. Willard FS, Douros JD, Gabe MB, et al. Tirzepatide is an imbalanced and biased dual GIP and GLP-1 receptor agonist. JCI Insight. 2020;5(17):e140532. doi: https://doi.org/10.1172/jci.insight.140532
10. Романцова Т.И. Тирзепатид — унимолекулярная полифармакология для лечения ожирения. // Эндокринология: новости, мнения, обучение. — 2025. — Т.14. — № 3. — C. 50-64. doi: https://doi.org/10.33029/2304-9529-2025-14-3-50-64
11. Müller TD, Finan B, Bloom SR, et al. Glucagon-like peptide 1 (GLP-1). Mol Metab. 2019;30:72-130. doi: https://doi.org/10.1016/j.molmet.2019.09.010
12. Müller TD, Adriaenssens A, Ahrén B, et al. Glucose-dependent insulinotropic polypeptide (GIP). Mol Metab. 2025;95:102118. doi: 10.1016/j.molmet.2025.102118
13. Campbell JE, Müller TD, Finan B, et al. GIPR/GLP-1R dual agonist therapies for diabetes and weight loss-chemistry, physiology, and clinical applications. Cell Metab. 2023;35(9):1519-1529. doi: https://doi.org/10.1016/j.cmet.2023.07.010
14. Gabery S, Salinas CG, Paulsen SJ, et al. Semaglutide lowers body weight in rodents via distributed neural pathways. JCI Insight. 2020;5(6):e133429. doi: https://doi.org/10.1172/jci.insight.133429
15. Samms RJ, Sloop KW. A Contemporary Rationale for Agonism of the GIP Receptor in the Treatment of Obesity. Diabetes. 2025: dbi240026. doi: https://doi.org/10.2337/dbi24-0026
16. Boer GA, Hay DL, Tups A. Obesity pharmacotherapy: incretin action in the central nervous system. Trends Pharmacol Sci. 2023;44(1):50-63. doi: https://doi.org/10.1016/j.tips.2022.11.001
17. O’Keefe JH, Franco WG, O’Keefe EL. Anti-consumption agents: Tirzepatide and semaglutide for treating obesity-related diseases and addictions, and improving life expectancy. Prog Cardiovasc Dis. 2025;89:102-112. doi: https://doi.org/10.1016/j.pcad.2024.12.010
18. James-Okoro PP, Lewis JE, Gribble FM, Reimann F. The role of GIPR in food intake control. Front Endocrinol (Lausanne). 2025;16:1532076. doi: https://doi.org/10.3389/fendo.2025.1532076
19. Douros JD, Flak JN, Knerr PJ. The agony and the efficacy: central mechanisms of GLP-1 induced adverse events and their mitigation by GIP. Front Endocrinol (Lausanne). 2025;16:1530985. doi: https://doi.org/10.3389/fendo.2025.1530985
20. Samms RJ, Cosgrove R, Snider BM, et al. GIPR Agonism Inhibits PYY-Induced Nausea-Like Behavior. Diabetes. 2022;71(7):1410-1423. doi: https://doi.org/10.2337/db21-0848
21. Urva S, Coskun T, Loghin C, et al. The novel dual glucosedependent insulinotropic polypeptide and glucagon-like peptide-1 (GLP-1) receptor agonist tirzepatide transiently delays gastric emptying similarly to selective long-acting GLP-1 receptor agonists. Diabetes Obes Metab. 2020;22(10):1886-1891. doi: https://doi.org/10.1111/dom.14110
22. Jalleh RJ, Plummer MP, Marathe CS, et al. Clinical Consequences of Delayed Gastric Emptying With GLP-1 Receptor Agonists and Tirzepatide. J Clin Endocrinol Metab. 2024;110(1):1-15. doi: https://doi.org/10.1210/clinem/dgae719. Erratum in: J Clin Endocrinol Metab. 2025;110(10):e3556. doi: https://doi.org/10.1210/clinem/dgaf387
23. Min JS, Jo SJ, Lee S, Kim DY, Kim DH, Lee CB, Bae SK. A Comprehensive Review on the Pharmacokinetics and Drug-Drug Interactions of Approved GLP-1 Receptor Agonists and a Dual GLP-1/GIP Receptor Agonist. Drug Des Devel Ther. 2025;19:3509-3537. doi: https://doi.org/10.2147/DDDT.S506957
24. Wong CK, McLean BA, Baggio LL, et al. Central glucagon-like peptide 1 receptor activation inhibits Toll-like receptor agonistinduced inflammation. Cell Metab. 2024;36(1):130-143.e5. doi: https://doi.org/10.1016/j.cmet.2023.11.009
25. Papakonstantinou I, Tsioufis K, Katsi V. Spotlight on the Mechanism of Action of Semaglutide. Curr Issues Mol Biol. 2024;46(12):14514-14541. doi: https://doi.org/10.3390/cimb46120872
26. Regmi A, Aihara E, Christe ME, et al. Tirzepatide modulates the regulation of adipocyte nutrient metabolism through long-acting activation of the GIP receptor. Cell Metab. 2024;36(7):1534-1549.e7. doi: https://doi.org/10.1016/j.cmet.2024.05.010
27. Yu X, Chen S, Funcke JB, et al. The GIP receptor activates futile calcium cycling in white adipose tissue to increase energy expenditure and drive weight loss in mice. Cell Metab. 2025;37(1):187-204.e7. doi: https://doi.org/10.1016/j.cmet.2024.11.003
28. Yaribeygi H, Maleki M, Jamialahmadi T, Sahebkar A. Anti-inflammatory benefits of semaglutide: State of the art. J Clin Transl Endocrinol. 2024;36:100340. doi: https://doi.org/10.1016/j.jcte.2024.100340
29. Badve SV, Bilal A, Lee MMY, Sattar N, Gerstein HC, et al. Effects of GLP-1 receptor agonists on kidney and cardiovascular disease outcomes: a meta-analysis of randomised controlled trials. Lancet Diabetes Endocrinol. 2025;13(1):15-28. doi: https://doi.org/10.1016/S2213-8587(24)00271-7
30. Vear A, Heneka MT, Clemmensen C. Incretin-based therapeutics for the treatment of neurodegenerative diseases. Nat Metab. 2025;7(4):679-696. doi: https://doi.org/10.1038/s42255-025-01263-4
31. Malhotra A, Grunstein RR, Fietze I, Weaver TE, Redline S, et al; SURMOUNT-OSA Investigators. Tirzepatide for the Treatment of Obstructive Sleep Apnea and Obesity. N Engl J Med. 2024;391(13):1193-1205. doi: https://doi.org/10.1056/NEJMoa2404881. Erratum in: N Engl J Med. 2024;391(15):1464. doi: https://doi.org/10.1056/NEJMx240005
32. Garvey WT, Mechanick JI, Brett EM, Garber AJ, Hurley DL, et al; Reviewers of the AACE/ACE Obesity Clinical Practice Guidelines. American Association of Clinical Endocrinologists and American College of Endocrinology Comprehensive Clinical Practice Guidelines For Medical Care of Patients With Obesity. Endocr Pract. 2016;22Suppl 3:1-203. doi: https://doi.org/10.4158/EP161365
33. Aronne LJ, Horn DB, le Roux CW, Ho W, Falcon BL, et al; SURMOUNT-5 Trial Investigators. Tirzepatide as Compared with Semaglutide for the Treatment of Obesity. N Engl J Med. 2025. doi: https://doi.org/10.1056/NEJMoa2416394
34. Lincoff AM, Brown-Frandsen K, Colhoun HM, Deanfield J, Emerson SS, et al; SELECT Trial Investigators. Semaglutide and Cardiovascular Outcomes in Obesity without Diabetes. N Engl J Med. 2023;389(24):2221-2232. doi: https://doi.org/10.1056/NEJMoa2307563
35. Zhao Z, Song J, Faurby M, et al. Lower Risk of MACE and All-Cause Death in Patients Initiated on Semaglutide 2.4 mg in Routine Clinical Care: Results from the SCORE Study (Semaglutide Effects on Cardiovascular Outcomes in People with Overweight or Obesity in the Real World). Moderated poster presentation presented at the American College of Cardiology Scientific Session & Expo 2025; 29-31 March 2025; McCormick Place Convention Center, Chicago, US. Presentation 947-13
36. Packer M, Zile MR, Kramer CM, Baum SJ, Litwin SE, et al; SUMMIT Trial Study Group. Tirzepatide for Heart Failure with Preserved Ejection Fraction and Obesity. N Engl J Med. 2025;392(5):427-437. doi: https://doi.org/10.1056/NEJMoa2410027
37. Kosiborod MN, Abildstrøm SZ, Borlaug BA, Butler J, Rasmussen S, et al; STEP-HFpEF Trial Committees and Investigators. Semaglutide in Patients with Heart Failure with Preserved Ejection Fraction and Obesity. N Engl J Med. 2023;389(12):1069-1084. doi: https://doi.org/10.1056/NEJMoa2306963
38. Malhotra A, Grunstein RR, Fietze I, Weaver TE, Redline S, et al; SURMOUNT-OSA Investigators. Tirzepatide for the Treatment of Obstructive Sleep Apnea and Obesity. N Engl J Med. 2024;391(13):1193-1205. doi: https://doi.org/10.1056/NEJMoa2404881. Erratum in: N Engl J Med. 2024;391(15):1464. doi: https://doi.org/10.1056/NEJMx240005
39. Bliddal H, Bays H, Czernichow S, Uddén Hemmingsson J, Hjelmesæth J, et al; STEP 9 Study Group. OnceWeekly Semaglutide in Persons with Obesity and Knee Osteoarthritis. N Engl J Med. 2024;391(17):1573-1583. doi: https://doi.org/10.1056/NEJMoa2403664
40. Loomba R, Hartman ML, Lawitz EJ, Vuppalanchi R, Boursier J, et al; SYNERGY-NASH Investigators. Tirzepatide for Metabolic Dysfunction-Associated Steatohepatitis with Liver Fibrosis. N Engl J Med. 2024;391(4):299-310. doi: https://doi.org/10.1056/NEJMoa2401943
41. Phase 3 ESSENCE Trial: Semaglutide in Metabolic DysfunctionAssociated Steatohepatitis. Gastroenterol Hepatol (N Y). 2024;20(12 Suppl 11):6-7
42. McGowan BM, Bruun JM, Capehorn M, Pedersen SD, Pietiläinen KH, et al; STEP 10 Study Group. Efficacy and safety of once-weekly semaglutide 2·4 mg versus placebo in people with obesity and prediabetes (STEP 10): a randomised, double-blind, placebo-controlled, multicentre phase 3 trial. Lancet Diabetes Endocrinol. 2024;12(9):631-642. doi: https://doi.org/10.1016/S2213-8587(24)00182-7
43. Jastreboff AM, le Roux CW, Stefanski A, Aronne LJ, Halpern B, et al; SURMOUNT-1 Investigators. Tirzepatide for Obesity Treatment and Diabetes Prevention. N Engl J Med. 2025;392(10):958-971. doi: https://doi.org/10.1056/NEJMoa2410819
44. Garvey WT, Frias JP, Jastreboff AM, le Roux CW, Sattar N, et al; SURMOUNT-2 investigators. Tirzepatide once weekly for the treatment of obesity in people with type 2 diabetes (SURMOUNT-2): a double-blind, randomised, multicentre, placebo-controlled, phase 3 trial. Lancet. 2023;402(10402):613-626. doi: https://doi.org/10.1016/S0140-6736(23)01200-X
45. Davies M, Færch L, Jeppesen OK, Pakseresht A, Pedersen SD, et al; STEP 2 Study Group. Semaglutide 2·4 mg once a week in adults with overweight or obesity, and type 2 diabetes (STEP 2): a randomised, double-blind, double-dummy, placebocontrolled, phase 3 trial. Lancet. 2021;397(10278):971-984. doi: https://doi.org/10.1016/S0140-6736(21)00213-0
Об авторах
Е. А. ТрошинаРоссия
Трошина Екатерина Анатольевна, д.м.н, член-корр. РАН, профессор
г. Москва, ул. Дмитрия Ульянова д. 11, 117292
М. Б. Анциферов
Россия
Анциферов Михаил Борисович, д.м.н., профессор
Москва
А. С. Аметов
Россия
Аметов Александр Сергеевич, д.м.н., профессор
Москва
Г. Р. Галстян
Россия
Галстян Гагик Радикович, д.м.н., проф.
Москва
Т. Н. Маркова
Россия
Маркова Татьяна Николаевна, д.м.н., проф.
Москва
Т. И. Романцова
Россия
Романцова Татьяна Ивановна, профессор, д.м.н.
Москва
Н. В. Мазурина
Россия
Мазурина Наталия Валентиновна, д.м.н.
Москва
О. М. Котешкова
Россия
Котешкова Ольга Михайловна, к.м.н.
Москва
Дополнительные файлы
|
|
1. Рисунок 1. Параметры, влияющие на выбор стартового препарата. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(460KB)
|
Метаданные ▾ | |
|
|
2. Рисунок 2. Исходные антропометрические параметры | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(399KB)
|
Метаданные ▾ | |
|
|
3. Рисунок 3. Выбор препарата для лечения ожирения в зависимости от предыдущего опыта применения или переносимости семаглутида | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(387KB)
|
Метаданные ▾ | |
|
|
4. Рисунок 4. Выбор препарата для лечения ожирения в зависимости от коморбидных состояний. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(277KB)
|
Метаданные ▾ | |
|
|
5. Рисунок 5. Алгоритм перехода с семаглутида 2,4 мг на тирзепатид у пациентов с ожирением + СД2. | |
| Тема | ||
| Тип | Исследовательские инструменты | |
Посмотреть
(279KB)
|
Метаданные ▾ | |
Рецензия
Для цитирования:
Трошина Е.А., Анциферов М.Б., Аметов А.С., Галстян Г.Р., Маркова Т.Н., Романцова Т.И., Мазурина Н.В., Котешкова О.М. Персонифицированный подход к терапии ожирения на основе доказательных данных и клинических алгоритмов: семаглутид или тирзепатид. Проблемы Эндокринологии. 2025;71(5):19-30. https://doi.org/10.14341/probl13677
For citation:
Troshina E.A., Antsiferov M.B., Ametov A.S., Galstyan G.R., Markova T.N., Romantsova T.I., Mazurina N.V., Koteshkova O.M. A personalized, evidence-based approach to obesity therapy using clinical algorithms: semaglutide or tirzepatide. Problems of Endocrinology. 2025;71(5):19-30. (In Russ.) https://doi.org/10.14341/probl13677
JATS XML

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).








































.jpg)


