Юбилей
Галина Афанасьевна Мельниченко — известный российский ученый-эндокринолог, один из ведущих в стране, автор и руководитель фундаментальных и прикладных исследований. Г.А. Мельниченко — один из лидеров создания методологии по организации эндокринологической службы Российской Федерации. Г.А. Мельниченко является одним из ведущих специалистов Российской Федерации по изучению заболеваний щитовидной железы, гипоталамо-гипофизарной системы, орфанных эндокринопатий, надпочечниковой патологии, синдромов множественных эндокринных неоплазий.
1 декабря 2021 года — юбилей у Валентины Александровны Петерковой, профессора, академика РАН, научного руководителя Института детской эндокринологии ФГБУ «НМИЦ эндокринологии» Минздрава России, главного внештатного специалиста детского эндокринолога Минздрава России, заслуженного врача Российской Федерации.
Редакционная статья
Эффективность системы здравоохранения во многом определяется кадровым составом и квалификацией врачей. Укомплектование персоналом медицинских организаций, в частности первичного звена, — важнейший аспект качества и доступности медицинской помощи, а также экономики в целом. Несмотря на имеющиеся кадровые проблемы эндокринологической службы, усиление роли государства в решении данного вопроса в виде долгосрочного стратегического планирования и повышения квалификации специалистов, увеличения объемов целевой подготовки врачей, а также их материальной и социальной поддержки позволяет надеяться на переход положительной динамики в уверенное разрешение кадрового кризиса.
ОБОСНОВАНИЕ. В соответствии с концепцией доказательной медицины методологическое качество исследования определяется двумя его аспектами: рисками систематических ошибок и рисками некорректности анализа данных. Минимизация обоих рисков повышает внутреннюю валидность исследования. Существуют многочисленные рекомендации и руководства по проведению статистического анализа данных в медицинских исследованиях и его представлению в публикациях, однако до настоящего времени международным сообществом не был выработан какой-либо формализованный вопросник для оценки качества статистического анализа, который был бы предназначен для рецензентов.
ЦЕЛЬ. Разработать инструмент формализованной оценки качества статистического анализа, представленного в научных медицинских публикациях.
МАТЕРИАЛЫ И МЕТОДЫ. Вопросник разработан на основе многолетнего опыта авторов в области статистического анализа данных и рецензирования статистических аспектов статей и диссертаций. При разработке вопросника принимались во внимание рекомендации SAMPL, документ ICH E9 и другие рекомендации. Выполнена внутренняя валидизация вопросника, заключавшаяся в проведении независимой оценки двумя экспертами 20 случайно отобранных в elibrary.ru статей о рандомизированных контролируемых испытаниях (РКИ), и дальнейшем статистическом анализе согласованности заключений экспертов.
РЕЗУЛЬТАТЫ. Разработан вопросник CORSTAN (CORrect STatistical ANalysis), состоящий из двух частей: первая часть (10 вопросов) предназначена для оценки исследований любых дизайнов, вторая (8 вопросов) – для дополнительной оценки РКИ. Предложена стратификация риска некорректности статистического анализа. Оценка внутренней валидности вопросника показала ее высокий уровень как в отношении согласованности оценок рецензентов по каждому из вопросов, так и в отношении оценки каждой из статей как по сумме баллов, так и по уровню риска некорректности статистического анализа.
ЗАКЛЮЧЕНИЕ. Использование вопросника и шкалы позволит упростить и гармонизировать статистическое рецензирование публикаций и рукописей в различных институциях – научных журналах, диссертационных советах и т.д. Вопросник также может быть полезен и авторам в процессе подготовки рукописей, он будет способствовать повышению качества не только публикаций, но и самих исследований. Мы планируем усовершенствовать вопросник по мере накопления опыта его применения.
Клиническая эндокринология
ОБОСНОВАНИЕ. За последние десятилетия микроРНК зарекомендовали себя как новые маркеры для целого ряда заболеваний. Определение специфичной панели микроРНК, отличающей пациентов с БИК и АКТГ-эктопированным синдромом (АКТГ-ЭС), смогло бы значительно упростить диагностику.
ЦЕЛЬ. Выявить циркулирующие микроРНК, отличающиеся у пациентов с БИК и АКТГ-ЭС в плазме крови, оттекающей от гипофиза.
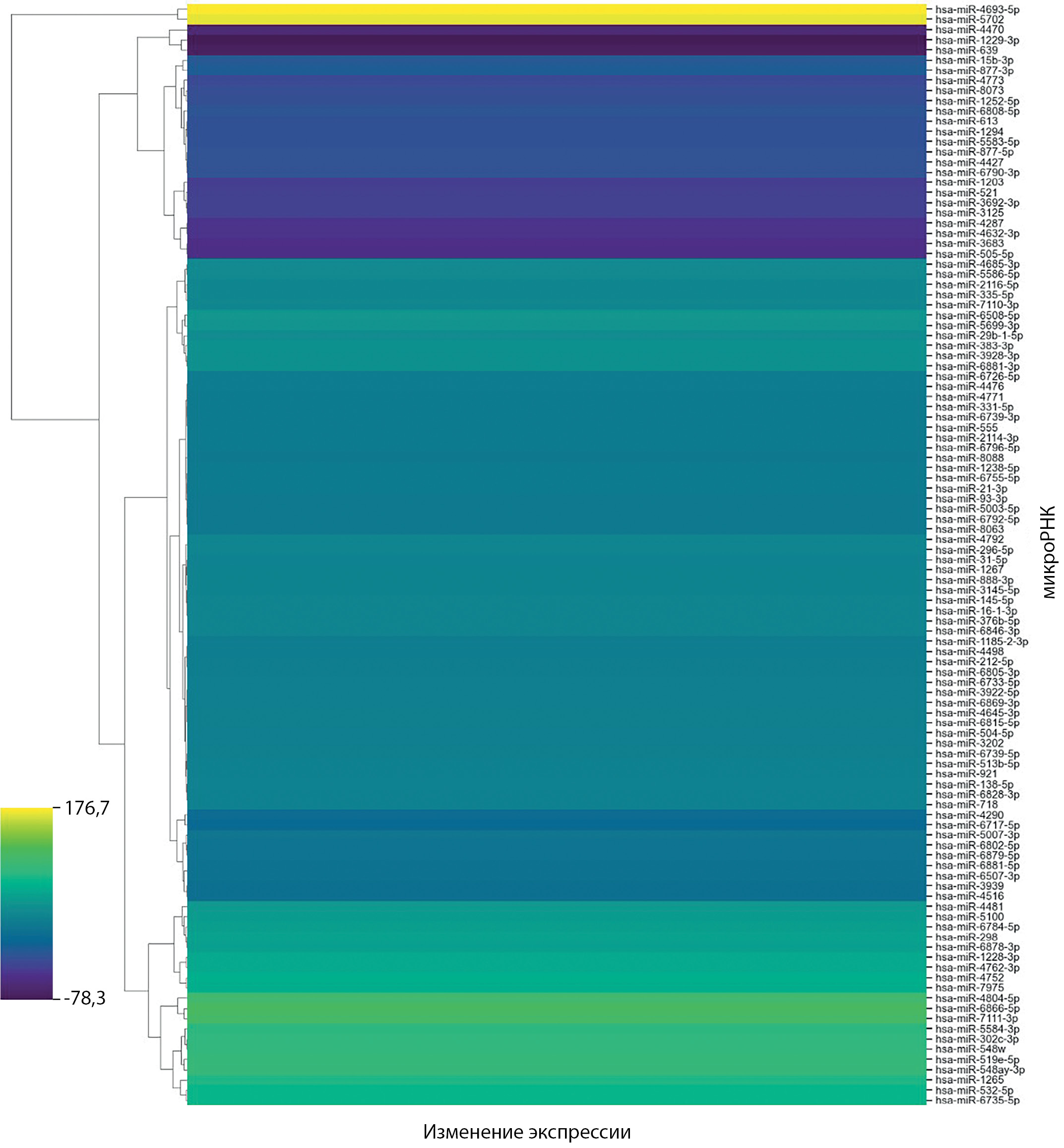
МАТЕРИАЛЫ И МЕТОДЫ. Выполнено одноцентровое, одномоментное, выборочное исследование случай-контроль. Включено 24 пациента с АКТГ-зависимым ЭГ, которым требовалось проведение селективного забора крови из нижних каменистых синусов (НКС). Из них 12 пациентов с БИК (м=2, ж=10), возрастная медиана 46,5 лет [33,8;53,5] и 12 пациентов с АКТГ-ЭС (м=4, ж=8), возрастная медиана 54 года [38,75;60,75]. Образцы плазмы крови из НКС были получены до введения стимуляционного агента, центрифугированы и заморожены при температуре -80С. Выделение микроРНК из плазмы крови проводили с помощью miRNeasy Serum/Plasma Kit («Qiagen», Германия) согласно инструкции компании-производителя на автоматической станции QIAcube («Qiagen», Германия). Концентрацию суммарной РНК в водном растворе оценивали на спектрофотометре NanoVue Plus («GE Healthcare», Великобритания). Библиотеки были подготовлены с помощью QIAseq miRNA Library Kit согласно стандартным протоколам производителя. Экспрессию микроРНК исследовали с помощью секвенирования на Illumina NextSeq 500 (Illumina NextSeq 500, США).
РЕЗУЛЬТАТЫ. Обнаружены 108 дифференциально экспрессирующихся микроРНК (p <0,05) после поправки на множественность сравнений. МикроРНК разделены на три группы – группа 1 с числом прочтений более 10 в обеих группах сравнения, группа 2 с числом прочтений менее 10 в одной из групп, группа 3 с числом прочтений менее 10 в обеих группах. Для верификации методом количественной ПЦР с обратной транскрипцией (RT-qPCR), планируется использовать следующие микроРНК: miR-383-3p, miR-4290 и miR-6717-5p, экспрессия которых была повышена у пациентов с БИК по сравнению с пациентами из группы АКТГ-ЭС в 46,36 раз (p=0,01), в 6,84 раз (p=0,036) и в 4,49 раз (p=0,031), соответственно, miR-1203, miR-1229-3p, miR-639, экспрессия которых была снижена у пациентов с БИК в 36,74 раз (p=0,013), в 78,3 раз (p=0,003), в 73,22 раза (p=0,002), соответственно, а также miR-302c-3p, экспрессия которой была повышена у пациентов с БИК в 92,69 раз (p=0,001).
ЗАКЛЮЧЕНИЕ. В ходе исследования был значительно расширен список микроРНК-кандидатов для диагностики АКТГ-зависимых форм ЭГ. Необходима валидизация полученных микроРНК в периферической крови на расширенной выборке пациентов методом RT-qPCR.
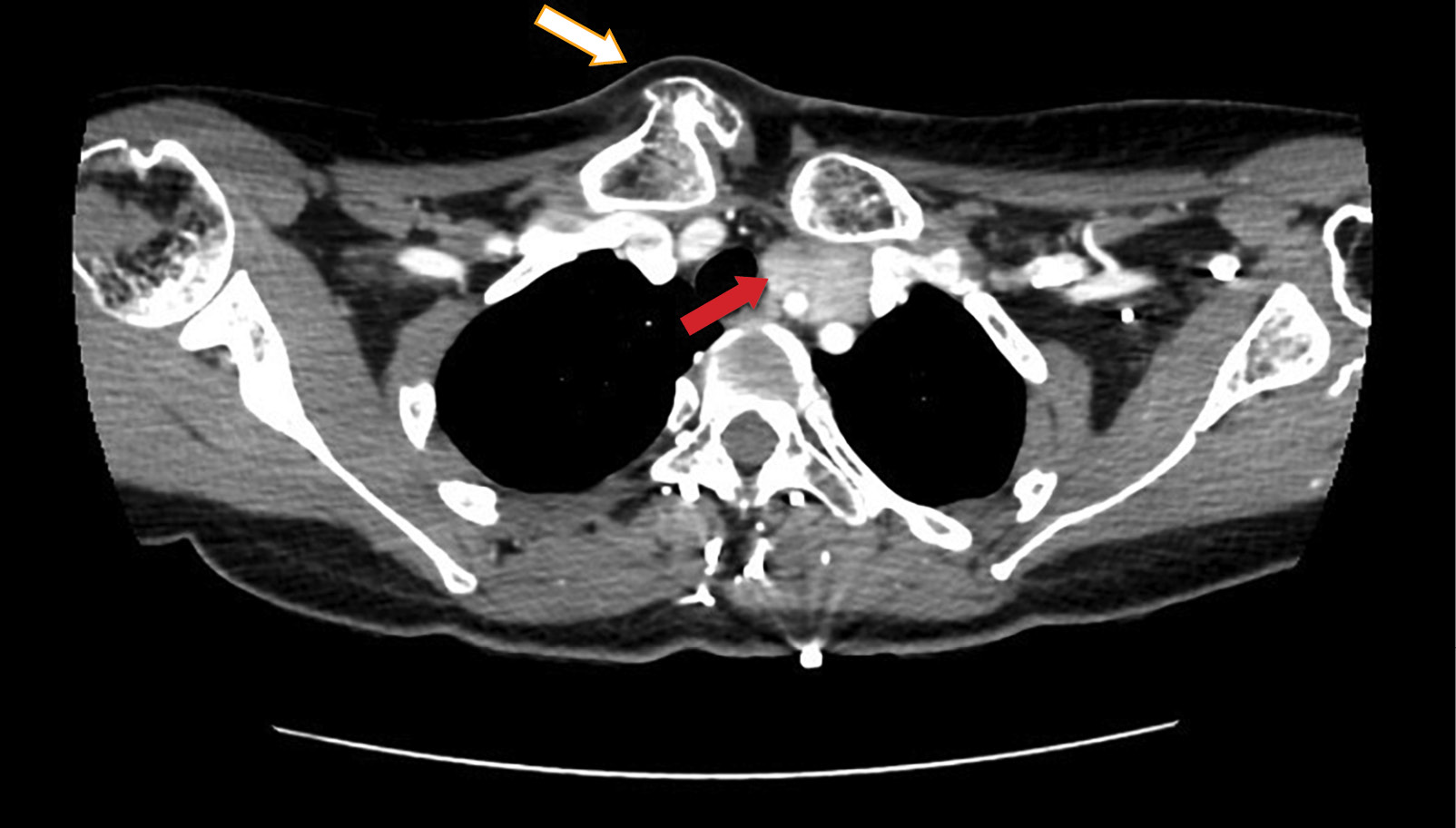
Полигландулярное поражение околощитовидных желез (ОЩЖ) при первичном гиперпаратиреозе (ПГПТ) может быть спорадическим или развиваться в рамках наследственных синдромов, манифестируя в молодом возрасте. Представлено описание тяжелой спорадической формы ПГПТ с гигантскими новообразованиями ОЩЖ у молодой пациентки. Клинические данные позволяли заподозрить МЭН-1 синдром или карциномы ОЩЖ, однако мутации CDKN, CDC73, MEN1 были исключены. Пациентке выполнено удаление трех выявленных опухолей: доброкачественных аденом левых ОЩЖ и гиперплазии правой ОЩЖ. Послеоперационная гипокальциемия и тяжелый синдром голодных костей потребовали назначения препаратов витамина D, карбоната кальция. Однако через год после операции подтвержден «мягкий» рецидив заболевания. С учетом отказа пациентки от повторной операции и значительного улучшения состояния органов-мишеней продолжено активное наблюдение. Пациентка нуждается в дальнейшем тщательном динамическом контроле специалистами с целью своевременного выявления показаний к повторному хирургическому лечению для улучшения качества и увеличения продолжительности жизни.
ОБОСНОВАНИЕ. Эффективный контроль аутоиммунного воспаления при болезни Грейвса предопределяет необходимость изучения дисфункции хелперных и цитотоксических Т-лимфоцитов, а также степени активации регуляторных Т-клеток при тиреостатической терапии болезни Грейвса, что позволит уточнить иммуномодулирующие эффекты длительной консервативной терапии тиамазолом и определить мишени для разработки современной таргетной терапии.
ЦЕЛЬ. Изучить фенотипический состав Т-лимфоцитов периферической крови у пациентов с болезнью Грейвса для оценки направленности иммунного ответа в зависимости от длительности медикаментозного эутиреоза.
МАТЕРИАЛЫ И МЕТОДЫ. Проведено одноцентровое одномоментное когортное сплошное открытое контролируемое исследование с оценкой фенотипического состава Т-клеток в периферической крови у женщин с болезнью Грейвса. Методом проточной цитометрии с использованием прямой иммунофлуоресценции с применением моноклональных антител были исследованы особенности фенотипа T-лимфоцитов в зависимости от продолжительности медикаментозного эутиреоза при консервативной терапии тиамазолом.
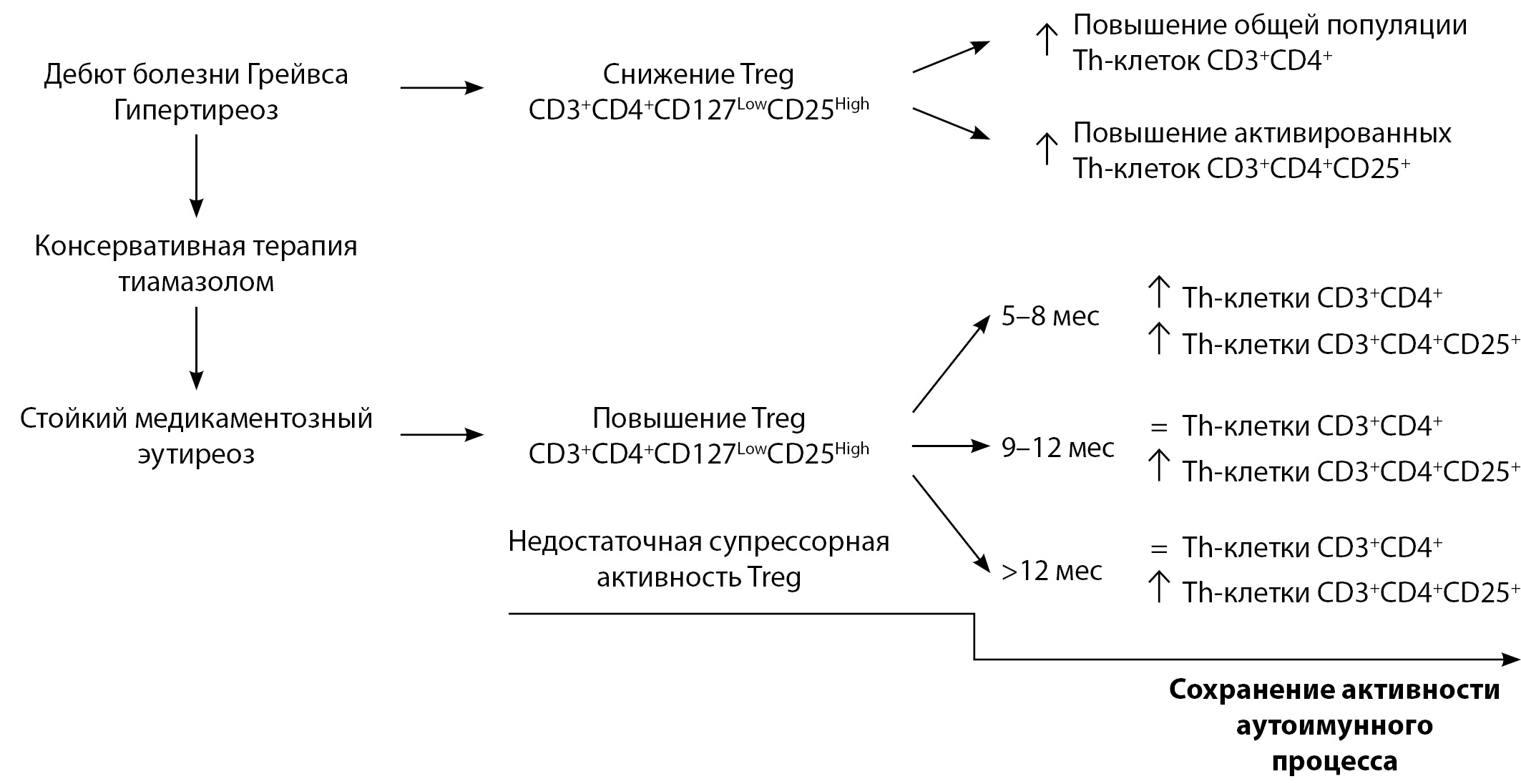
РЕЗУЛЬТАТЫ. В исследование включены 135 женщин с верифицированным диагнозом болезни Грейвса, средний возраст 43,09±12,81 года, из них 120 (88,91%) — с рецидивом заболевания и 15 (11,09%) — с впервые выявленным гипертиреозом. Установлено повышение процентного содержания активированных Т-хелперов (CD3+CD4+CD25+) у больных болезнью Грейвса с продолжительностью медикаментозного эутиреоза от 5 до 8 мес и от 9 до 12 мес соответственно, Me=0,94 (0,48–1,45; p=0,020) и Me=0,95 (0,41–1,80; p=0,025), у лиц контрольной группы — Ме=0,12 (0,03-0,68). Установлено повышение количества регуляторных Т-лимфоцитов (CD4+CD25+CD127Low) как в группе больных с продолжительностью медикаментозного эутиреоза от 5 до 8 мес (Me=3,01 (1,88–4,47); p=0,024), так и у пациентов с длительностью медикаментозного эутиреоза от 9 до 12 мес (Me=5,52 (2,77–11,61); p<0,001) в сравнении с показателями группы контроля (Ме=1,81 (0,91-2,82)). Уровень регуляторных Т-клеток в периферической крови пациентов с болезнью Грейвса с продолжительностью медикаментозного эутиреоза более 12 мес снижается, но сохраняется повышенным относительно контроля.
ЗАКЛЮЧЕНИЕ. У пациентов с болезнью Грейвса с продолжительностью медикаментозного эутиреоза от 5 до 8 мес и от 9 до 12 мес повышается популяция регуляторных Т-лимфоцитов с фенотипом CD4+CD25+CD127Low. Количество активированных Т-хелперов с фенотипом CD3+CD4+CD25+ сохраняется повышенным независимо от продолжительности медикаментозного эутиреоза. У пациентов с болезнью Грейвса с продолжительностью медикаментозного эутиреоза более 12 мес сохраняется компенсаторное повышение регуляторных Т-лимфоцитов, а общее количество Т-хелперов восстанавливается до уровня контроля.
ОБОСНОВАНИЕ. Синдром множественных эндокринных неоплазий 1 типа (МЭН 1) — это редкое аутосомно-доминантное заболевание, обусловленное мутациями в гене MEN1, кодирующем белок менин. В случае выявления у пациента фенотипа МЭН 1 при отсутствии мутаций в гене MEN1 состояние расценивается как фенокопия данного синдрома. Хотя в понимании функции менина был достигнут значительный прогресс, его значение в онкогенезе эндокринных желез все еще выясняется. Благодаря ключевой роли этого гена в физиологических и патологических процессах оценка экспрессии менина может дать ценную информацию.
ЦЕЛЬ. Определить, имеются ли какие-либо различия в экспрессии менина в тканях аденом гипофиза (АГ) у пациентов с фенокопиями синдрома МЭН 1 и генетически подтвержденным МЭН 1 по сравнению с их спорадическими формами.
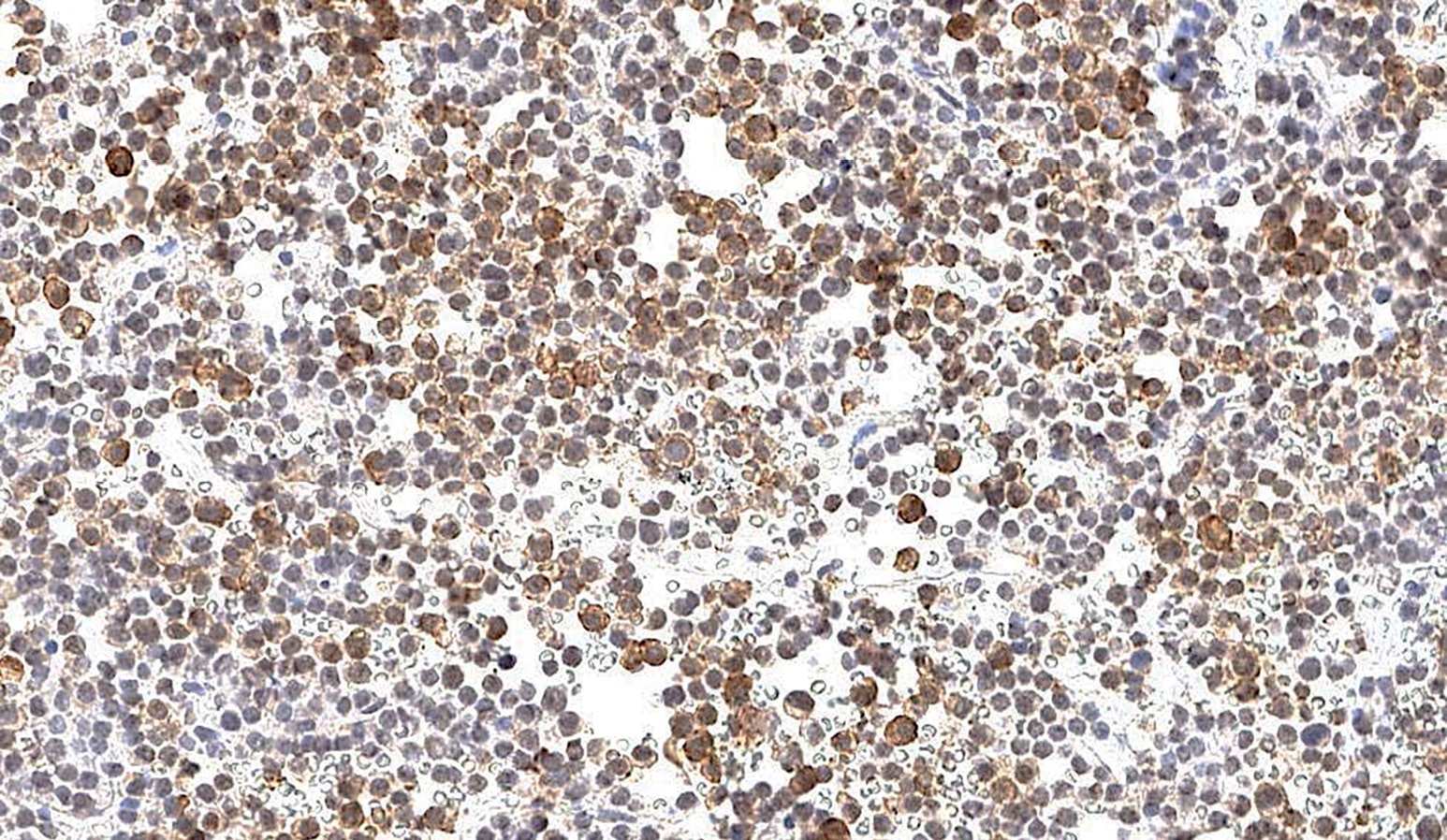
МАТЕРИАЛЫ И МЕТОДЫ. Проведено одномоментное одноцентровое исследование: иммуногистохимическая (ИГХ) оценка экспрессии менина и типа секреции опухолей гипофиза пациентов с генетически подтвержденным МЭН 1 (гМЭН 1), фенокопиями МЭН 1 (фМЭН 1) и спорадической акромегалией (СА), оперированных в 2008–2020 гг. ИГХисследование выполнено при использовании антител к менину, пролактину, соматотропному, адренокортикотропному, фолликулостимулирующему, тиреотропному гормонам, Pit-1, T-box, ERA на заранее подготовленных срезах толщиной 3–4 мкм.
РЕЗУЛЬТАТЫ. В исследование было включено 35 образцов опухолей гипофиза: гМЭН 1 — 9 образцов, фМЭН 1 — 12, CA — 14. Пациенты трех групп были сопоставимы по полу, размерам АГ, приему лекарственных препаратов. Группа гМЭН 1 отличалась от фМЭН 1 и СА по возрасту (р=0,0005). У пациентов с гМЭН 1 экспрессия менина варьировала от отсутствия окрашивания (5/9) до интенсивного окрашивания цитоплазмы. В группе фМЭН 1 в основном присутствовала цитоплазматическая экспрессия менина (11/12). В группе СА окраска отсутствовала в 1 случае, ядерная экспрессия была выявлена в 6/14 случаев. Группа фМЭН 1 показала значительно большую цитоплазматическую экспрессию менина, чем в группе гМЭН 1 (p=0,006). Группа гМЭН 1 также отличалась от группы СА по экспрессии менина (р=0,012). Статистически значимых различий между группами фМЭН 1 и СА выявлено не было (p=0,049).
ЗАКЛЮЧЕНИЕ. По результатам исследования оценки экспрессии менина выявлено, что экспрессия в целом сохранена в АГ у фМЭН 1 и СА, хотя и с разной локализацией в структуре клетки (ядро и/или цитоплазма). В то же время экспрессия менина сильно варьирует в АГ у пациентов с гМЭН 1. По полученным данным можно предположить, что патогенез АГ при фМЭН 1 и СА может иметь сходство, однако, по всей видимости, имеются факторы, способствующие появлению нескольких опухолей эндокринных желез у одного человека с фМЭН 1. Для понимания процесса необходимо дальнейшее исследование ассоциированных с МЭН 1 генов, эпигенетических факторов, сигнальных путей, в которых участвует менин.
Ядерная медицина (ЯМ) – медицинская специальность, использующая радионуклиды (радиоактивные “трейсеры”) и ионизирующее излучение с диагностико-терапевтической (тераностической) целью. ЯМ возникла и развивается на стыке физики, химии и клинической медицины. Излучение, испускаемое радиоактивными изотопами, может состоять из гамма-лучей, бета- и альфа-частиц или их комбинации. Выбор радиоизотопа для медицинских целей осуществляется в соответствии со следующими требованиями: низкая радиотоксичность, подходящий тип радиоактивного излучения, энергия и период полураспада (от нескольких минут до нескольких часов и дней), а также удобное для регистрации гамма-излучение. Радионуклид входит в состав радиофармацевтического лекарственного препарата (РФЛП) и выполняет роль его маркера. РФЛП накапливается в анатомических структурах, становится переносчиком координированной информации от пациента к гамма-камере или другому медицинскому прибору и отражает динамику процессов, протекающих в исследуемом органе. В 2021 году ЯМ отмечает 80-летний юбилей. Траектория развития ЯМ объединяет современные методы радиотераностики, включая прикладные геномные и постгеномные технологии.
ОБОСНОВАНИЕ. Дефицит (<20 нг/мл) и недостаточность (20–29 нг/мл) витамина D (25-гидроксивитамина D [25(ОН)D]) часто встречаются при первичном гиперпаратиреозе (ПГПТ), но данные о метаболизме витамина D в этой популяции ограничены.
ЦЕЛЬ. Изучение метаболитов витамина D и их взаимосвязи с основными показателями фосфорно-кальциевого обмена у пациентов с верифицированным ПГПТ исходно и на фоне однократного перорального приема колекальциферола в болюсной дозе (150 000 МЕ).
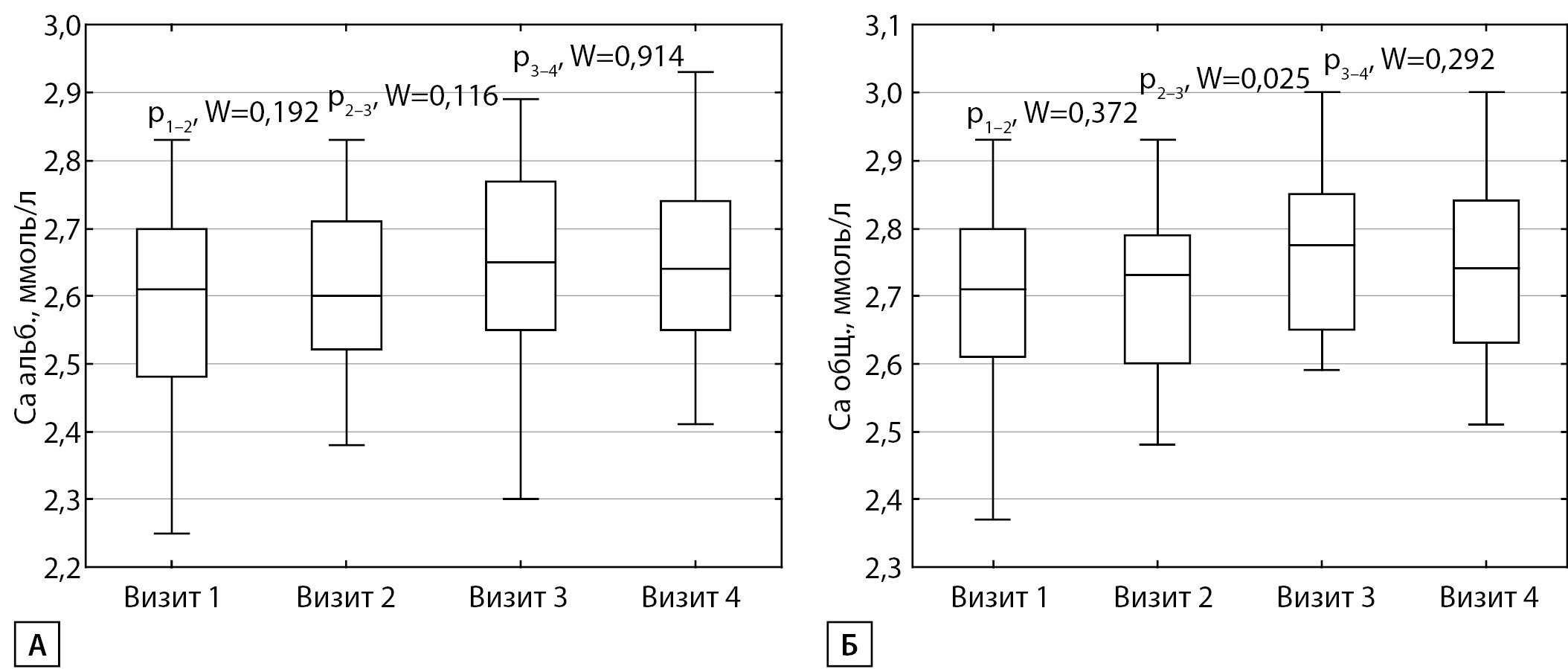
МАТЕРИАЛЫ И МЕТОДЫ. Проведено одноцентровое интервенционное динамическое проспективное сравнительное исследование. В исследование вошли 54 человека, распределенных по двум группам: в 1-ю группу включены 27 пациентов с подтвержденным ПГПТ, для сравнения была сформирована 2-я контрольная группа (n=27), сопоставимая по полу (р=0,062). Исследование включало 4 визита, на визите 1 выполнялись лабораторное обследование и прием болюсной дозы колекальциферола, на последующих визитах — динамическое лабораторное обследование.
РЕЗУЛЬТАТЫ. Дефицит витамина D (менее 20 нг/мл) определялся у 69% пациентов с ПГПТ. В группе ПГПТ перед приемом колекальциферола наблюдалась прямая ассоциация 1,25(OH)2 D3 с альбумин-скорректированным и ионизированным кальцием, а также между отношением 25(OH)D3 /24,25(OH)2 D3 с паратиреоидным гормоном (ПТГ) и магнием. После приема болюсной дозы колекальциферола на всех визитах в группе ПГПТ уровни 1,25(ОН)2 D3 и соотношение 25(OH)D3 /24,25(OH)2 D3 значимо увеличивались, а 25(OH)D3 /1,25(OH)2 D3 — снижались. При сопоставимой с контролем концентрации 25(OH)D уровни 1,25(OH)2 D3 у пациентов с ПГПТ были исходно на 55% выше, а после приема 150 000 МЕ повышались к 3–7-му дню на дополнительные 23–36%, что на каждом визите было значимо выше таковых значений в группе контроля: 44, 74 и 65% на визите 2, 3 и 4 соответственно (р< 0,05). Использование насыщающих доз в группе ПГПТ не приводило к значимому нарастанию гиперкальциемии и гиперкальциурии, что свидетельствует о безопасности использования данной схемы у пациентов с исходно мягкой гиперкальциемией (альбумин-скорректированный кальций <3 ммоль/л). После приема болюсной дозы колекальциферола ни у одного из участников исследования не фиксировались побочные явления.
ЗАКЛЮЧЕНИЕ. Впервые проведена комплексная оценка метаболитов витамина D у пациентов с ПГПТ до и после использования болюсной дозы колекальциферола. Полученные результаты свидетельствуют об особенностях метаболизма витамина D при хронической избыточной секреции ПТГ, что безусловно, значимо для понимания патогенеза заболевания, и в дальнейшем эти данные могут быть использованы для разработки терапевтических схем по назначению колекальциферола в указанной популяции.
Экспериментальная эндокринология
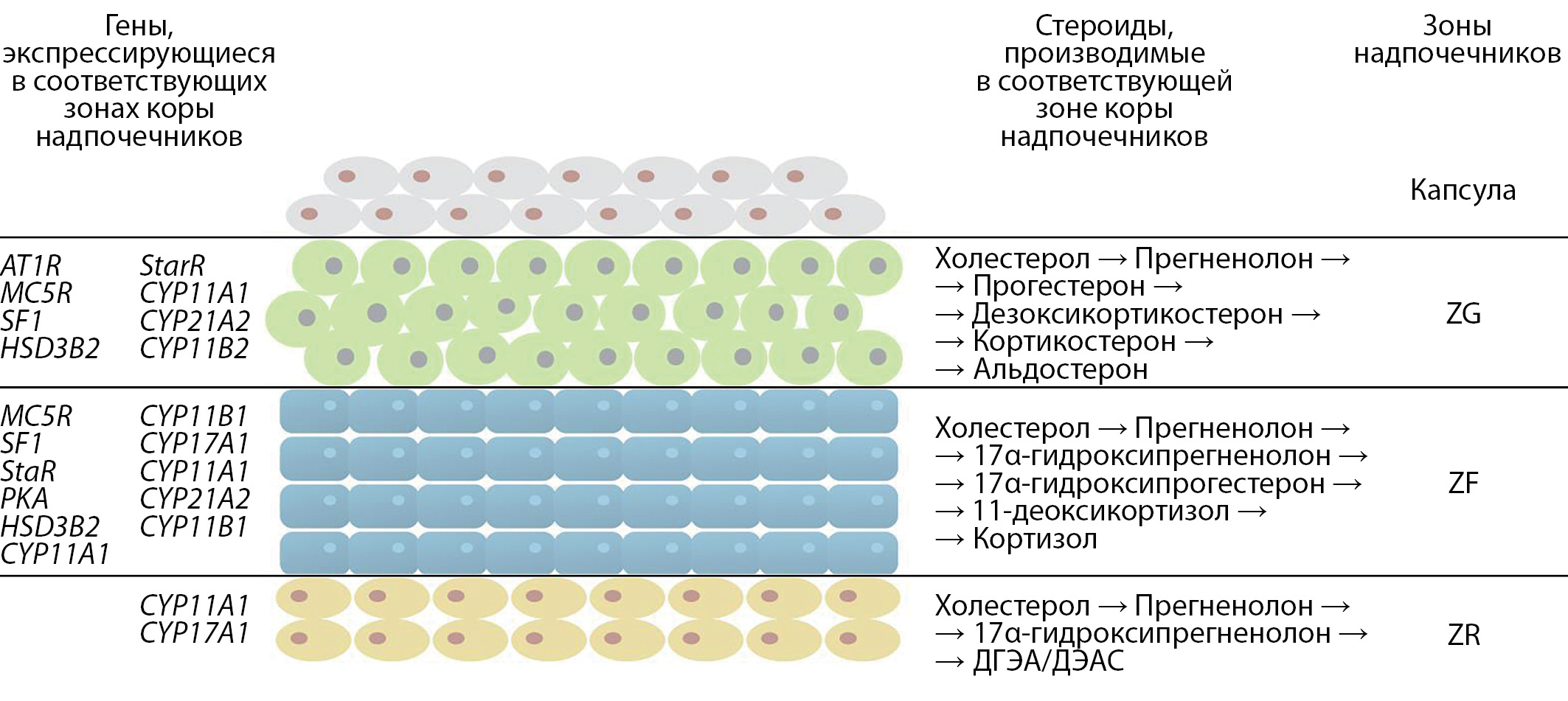
Современное понимание организации работы тканей и органов на молекулярном уровне в норме и патологии открывает существенные перспективы для разработки новых, принципиально иных подходов к лечению различных заболеваний. В частности, моногенные наследственные заболевания перестают быть приговором — появившиеся в последнее десятилетие методы геномного редактирования сейчас активно исследуются как инструменты для исправления мутаций в пораженных органах. В свою очередь, появляются новые протоколы получения различных типов клеток и клеточных систем человека и животных, отражающих реальные структуры in vivo. Все эти методы, а также совмещение генной и клеточной терапии активно разрабатываются, и некоторые подходы уже сейчас проходят клинические испытания. Надпочечниковая недостаточность, вызванная разными причинами, также может стать объектом разработки такого рода терапевтических стратегий. Надпочечники представляют собой сложно организованный орган, разные структурные части которого взаимодействуют друг с другом посредством сложной координации эндокринных и паракринных сигналов. В данном обзоре суммированы результаты исследований структурной организации и функционирования надпочечников на молекулярном уровне и современные подходы к лечению патологии надпочечников.
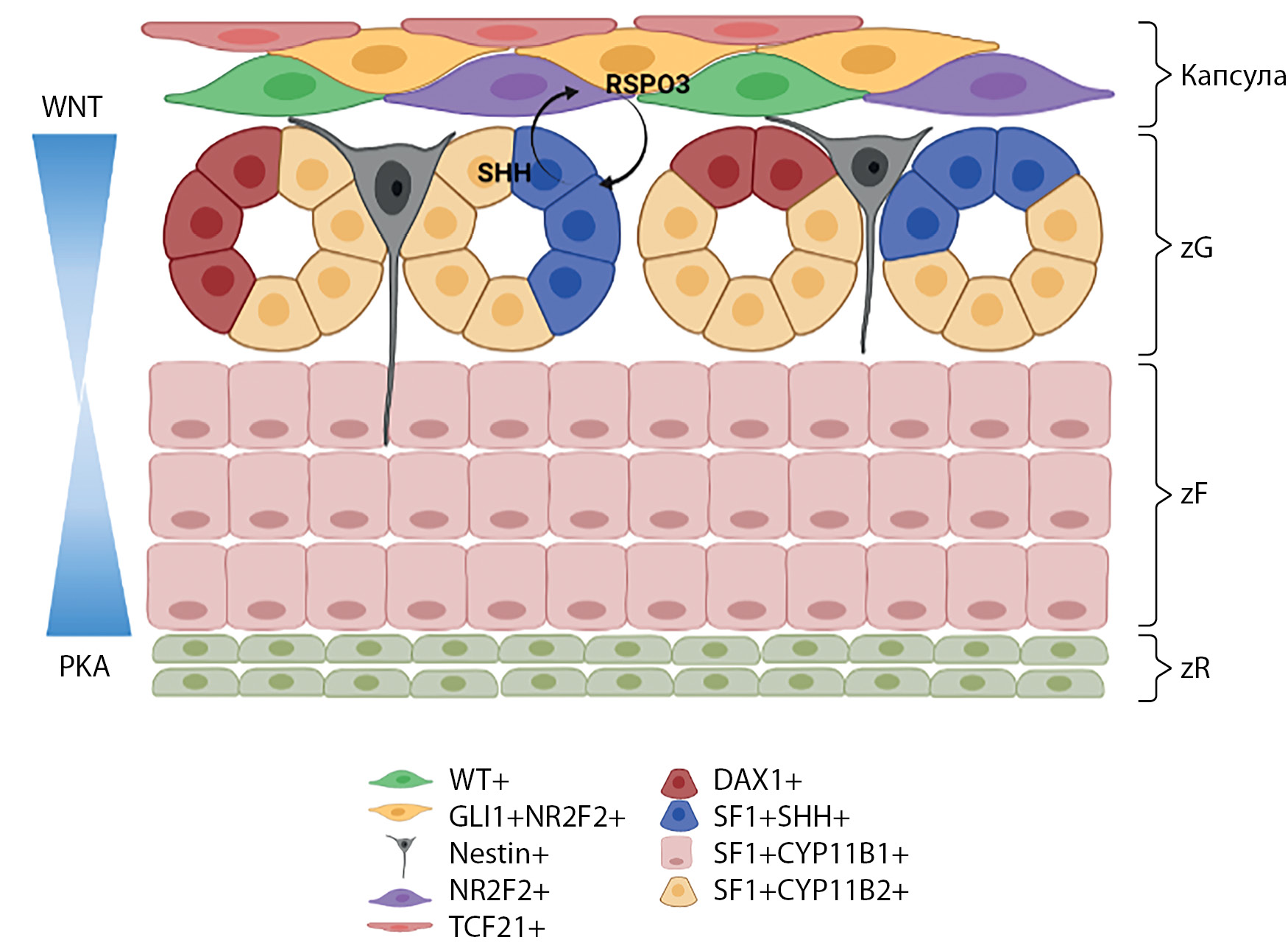
Стволовые клетки взрослого организма вызывают сегодня большой интерес ввиду активного развития клеточных и геномных технологий. Именно они являются мишенью новых терапевтических подходов, основанных на редактировании мутаций или восполнении органов, поврежденных в результате аутоиммунной реакции, старения и прочих патологических процессов. Также стволовые клетки, в том числе пациент-специфичные (индуцированные плюрипотентные стволовые клетки), и полученные путем дифференцировки из них культуры тканей и органоидов являются наиболее приближенными к in vivo моделями человеческого организма, что позволяет получать более релевантные данные по тестированию различных терапевтических подходов и фармакологических препаратов. В представленном обзоре описаны основные молекулярные пути, ответственные за поддержание гомеостаза коры надпочечников — сложного, структурно и функционально неоднородного органа. Кора надпочечников обновляется в течение онтогенеза организма за счет пула клеток-предшественниц (стволовых клеток и прогениторов), находящихся в тесном контакте с дифференцированными стероидогенными клетками и подвергающихся постоянному контролю эндокринных и паракринных сигналов. Понимание путей сигналинга и взаимодействия разных типов клеток позволит разработать наиболее подходящие протоколы получения клеток коры надпочечников на разных стадиях дифференцировки для использования их в научных и медицинских целях.
Болезни костной и жировой ткани
Жировая ткань, состоящая из различных видов жира, является в организме одним из самых больших эндокринных органов, играющим множество ролей, которые включают, но не ограничиваются сохранением энергетических запасов, метаболическим гомеостазом, продукцией тепла, участием в иммунных функциях и секрецией целого ряда биологически активных факторов, называемых адипокинами. Самым обильно секретируемым из адипокинов является адипонектин. Этот вырабатываемый адипоцитами гормон оказывает плейотропное действие и обладает способностью повышать чувствительность к инсулину, а также демонстрирует антидиабетические свойства и эффекты противодействия развитию ожирения, воспаления, атеросклероза и, кроме того, еще и проявляет кардио- и нейропротективные свойства. С другой стороны, помимо вышеперечисленных защитных свойств и возможности предотвращения развития различных патологических процессов в разных типах клеток, адипонектин может быть связан с развитием ряда системных заболеваний и злокачественных опухолей. Снижение уровней адипонектина, как оказалось, наблюдается в том числе при дыхательной недостаточности, связанной с коронавирусной инфекцией COVID-19, что обусловлено в основном развитием феномена, называемого «адипонектиновый парадокс». Многочисленные доказательства многоликости функций адипонектина в организме были получены в ходе исследований на животных моделях, больше всего на грызунах. Наш краткий обзор полностью посвящен многофункциональной роли адипонектина и механизмам его действия при различных физиологических и патологических состояниях.
Детская эндокринология
ОБОСНОВАНИЕ. Терапия сахарного диабета 1 типа (СД1), до настоящего времени является во многом не решенной клинической проблемой. Несмотря на внедрение в клиническую практику современных препаратов инсулина, устройств для его введения, а также непрерывного мониторинга уровня глюкозы, цели терапии зачастую не достигаются. При этом, международная федерация диабета (IDF) отмечает рост распространенности и заболеваемости СД1 у детей и подростков в мире. Федеральный регистр сахарного диабета (ФРСД) – динамически обновляющаяся база данных больных СД, которая позволяет оценить показатели распространенности и заболеваемости, степень достижение целей гликемического контроля, а также частоту развития осложнений СД.
ЦЕЛЬ. Анализ эпидемиологических данных СД1 (распространенности, заболеваемости) у детей и подростков (пациенты с рождения до 18 лет) Москвы по данным ФРСД и оценка их динамики, а также динамики достижения целей гликемического контроля и частоты встречаемости осложнений СД1 за 2015-2020 гг.
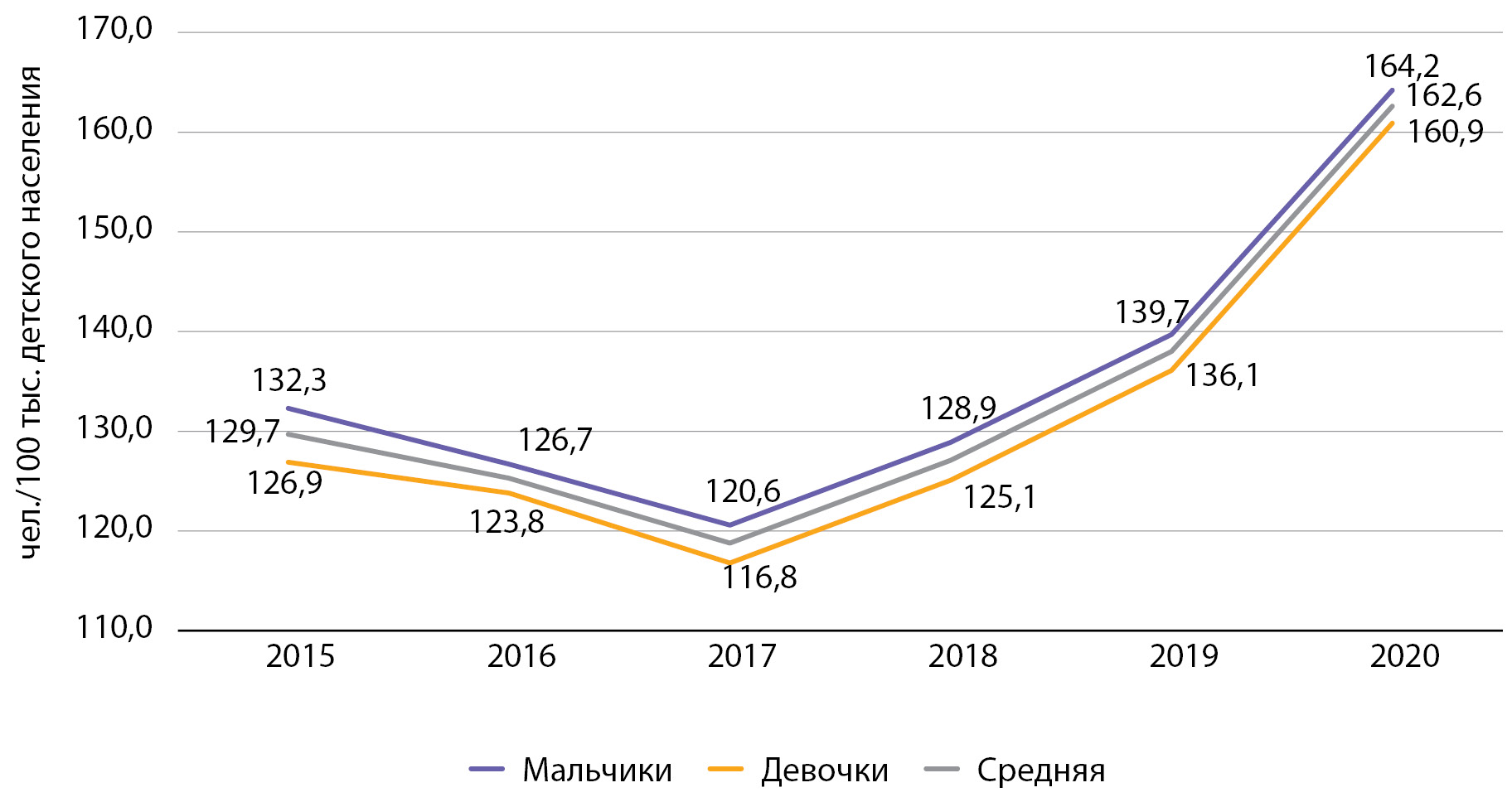
МАТЕРИАЛЫ И МЕТОДЫ. Объект исследования – выборка из базы данных Московского сегмента ФРСД когорты пациентов с СД1 моложе 18 лет, состоявших на учете за период 01.01.2015-01.01.2021 гг. Эпидемиологические показатели распространенности и заболеваемости рассчитаны на 100 тыс. соответствующего населения.
РЕЗУЛЬТАТЫ. численность детей и подростков, страдающих СД1 в Москве на 01.01.2021 г. составила 4024 чел. (2962 ребенка и 1062 подростка). За период с 2015 – 2020 гг., отмечался рост распространенности СД1 (возможно за счет повышения качества регистрации данных в ФРСД) и снижение заболеваемости как среди детей, так и среди подростков. Также отмечалось снижение уровня НвА1с и доли пациентов с НвАс1 > 8,0% среди детей с СД1. Как среди детей, так и среди подростков с СД1 отмечалось снижение частоты диабетических ком и кетоацидозов с одновременным ростом частоты тяжелых гипогликемий, а также снижение частоты ретинопатии, нефропатии. При этом, частота нейропатии снижалась среди детей и увеличивалась среди подростков.
ЗАКЛЮЧЕНИЕ. Полученные данные динамического ведения подростков с СД1 являются основанием для рассмотрения вопроса разработки профильной программы их динамического наблюдения, с учетом необходимости психологической и социальной поддержки пациентов и членов их семей.
Ошибки
В статье «Клинические и молекулярно-генетические характеристики пациентов с нарушением формирования пола 46,XY, обусловленным мутациями в гене NR5A1», опубликованной в Т. 66 № 3 журнала «Проблемы Эндокринологии» за 2020 г. (doi: 10.14341/probl12445), допущены ошибки:
- в аннотации «Среди обнаруженных мутаций 15 ранее описаны не были» была исправлена информация на «Среди обнаруженных мутаций 22 ранее описаны не были»;
- в подразделе РЕЗУЛЬТАТЫ «У 36 пациентов было выявлено 31 вариант в гене NR5A1, 15 из которых ранее описаны не были» внесены изменения на «У 36 пациентов было выявлено 31 вариант в гене NR5A1, 22 из которых ранее описаны не были»;
- в подразделе РЕЗУЛЬТАТЫ «Среди впервые выявленных вариантов изменений в гене NR1A1 два приводят к образованию стоп-кодона – p.Y197X и p.Y25X, два к сдвигу рамки считывания — p.N385SfsX10 и p.L245AfsX53, что не позволяет сомневаться в их патогенности. Среди ранее неописанных вариантных изменений 5 миссенсмутаций (p.C283Y, p.С283F, p.H24Q, p.M126K, p.A82T) и 1 синонимичная замена, затрагивающая сайт сплайсинга (E330E), были оценены как патогенные, а 5 других — как вероятно патогенные» была исправлена информация на «Среди впервые выявленных вариантов изменений в гене NR1A1 два приводят к образованию стоп-кодона — p.Y197X и p.Y25X, два к сдвигу рамки считывания — p.N385SfsX10 и p.L245AfsX53, что не позволяет сомневаться в их патогенности. Среди ранее неописанных вариантных изменений 5 миссенс-мутаций (p.C283Y, p.С283F, p.H24Q, p.M126K, p.A82T ) и 1 синонимичная замена, затрагивающая сайт сплайсинга (E330E), были оценены как патогенные, а 5 других — как вероятно патогенные»;
- внесены исправления в таблицу 2. Приведенная ранее информация в статье не должна была сколь-нибудь существенно отразиться на восприятии информации читателями и/или интерпретации представленных данных. Авторы выражают сожаления за неверную информацию в опубликованной ранее статье.

Контент доступен под лицензией Creative Commons Attribution-NonCommercial-NoDerivatives 4.0 International License (CC BY-NC-ND 4.0).
ISSN 2308-1430 (Online)










































.jpg)


